Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nNO = 0,15 (mol)
Gọi a là số mol Cu trong X đã phản ứng. Gọi b là số mol Fe3O4 trong X
Ta có: 64a + 232b = 61,2 – 2,4
Các nguyên tố Cu, Fe, O trong hỗn hợp X khi phản ứng với HNO3 chuyển thành muối Cu2+, Fe2+ (vì dư kim loại), H2O do đó theo bảo toàn e: 2a + 2.3b – 2.4b = 3.0,15
Từ đó: a = 0,375; b = 0,15
Muối khan gồm có: Cu(NO3)2 (a = 0,375 mol) và Fe(NO3)2 (3b = 0,45 mol)
mmuối = 188.0,375 + 180.0,45 = 151,5 (gam)
Đáp án B

nCu= 0,12 mol; nHNO3= 0,12 mol; nH2SO4= 0,1 mol
3Cuhết + 8H+hết + 2NO3-dư® 3Cu2+ + 2NO + 4H2O
0,12 0,32 0,12 ® 0,12
nNO3- dư= 0,12- 0,12.2/3= 0,04 mol
Muối khan thu được có chứa: 0,12 mol Cu2+, 0,04 mol NO3- và 0,1 mol SO42-
→ m muối khan= 0,12.64+ 0,04.62+ 0,1.96= 19,76 gam


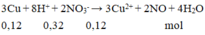



nFe=\(\dfrac{16,8}{56}=0,3mol\)
\(n_{H_2SO_4}=\dfrac{78,4}{98}=0,8mol\)
2Fe+6H2SO4\(\rightarrow\)Fe2(SO4)3+3SO2+6H2O
-Tỉ lệ: \(\dfrac{0,3}{2}=0,15>\dfrac{0,8}{6}\approx0,133\)\(\rightarrow\)Fe dư
\(n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{6}n_{H_2SO_4}=\dfrac{0,8}{6}=\dfrac{0,4}{3}mol\)
\(n_{Fe\left(pu\right)}=\dfrac{2}{6}n_{H_2SO_4}=\dfrac{2}{6}.0,8=\dfrac{1,6}{6}mol\)
\(n_{Fe\left(dư\right)}=0,3-\dfrac{1,6}{6}=\dfrac{17}{30}mol\)
Fe+Fe2(SO4)3\(\rightarrow\)3FeSO4
-Tỉ lệ: \(\dfrac{1,6}{6}\approx0,26< \dfrac{17}{30}\approx0,56\)\(\rightarrow\)Fe2(SO4)3 dư
Fe+Fe2(SO4)3\(\rightarrow\)3FeSO4
\(\dfrac{1,6}{6}\rightarrow\)\(\dfrac{1,6}{6}\)............0,8
\(n_{Fe_2\left(SO_4\right)_3\left(dư\right)}=\dfrac{17}{30}-\dfrac{1,6}{6}=0,3mol\)
mmuối=\(m_{FeSO_4}+m_{Fe_2\left(SO_4\right)_3}=0,8.152+0,3.400=121,216gam\)
Mơn bn nhìu ạ