Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Gọi số khối của hai đồng vị X, Y là A1 và A2; phần trăm số nguyên tử của hai đồng vị này là x1 và x2. Theo giả thiết ta có:
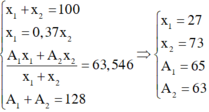

Đáp án B
Chọn số lượng nguyên tử Y là 100 thì số lượng nguyên tử X là 37.
Gọi số khối của X là A thì số khối của Y là (128 – A).
Do đó nguyên tử khối trung bình của Cu là:
M ¯ = 37 A + 100 ( 128 - A ) 37 + 100 = 63 , 54 ⇔ A = 65
Vậy số khối của X và Y lần lượt là 65 và 63.

Chọn số lượng nguyên tử Y là 100 thì số lượng nguyên tử X là 37.
Gọi số khối của X là A thì số khối của Y là (128 – A).
Do đó nguyên tử khối trung bình của Cu là:
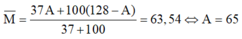
Vậy số khối của X và Y lần lượt là 65 và 63.
Đáp án D

Đáp án B.
Gọi số khối của hai đồng vị X, Y là A1 và A2; phần trăm số nguyên tử của hai đồng vị này là x1 và x2. Theo giả thiết ta có:
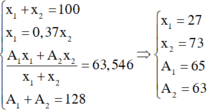

Đáp án A
Gọi số khối của đồng vị X, Y lần lượt là x, y
Chú ý Số nguyên tử đồng vị X = 0,37 số nguyên tử đồng vị Y nên nếu có 1 nguyên tử Y thì có 0,37 nguyên tử X
Ta có hệ:
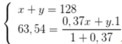
⇒
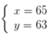
Vậy số notron của đồng vị Y hơn số notron của đồng vị X là : 65- 63 = 2
a)Đặt công thức muối là MCln x mol
\(MCl_n+nAgNO_3\rightarrow nAgCl+M\left(NO_3\right)_n\)
\(n_{MCl_n}=\dfrac{100\%.n_{AgCl}}{96\%.n}=\dfrac{100\%.0,2112}{96\%.n}=\dfrac{0,22}{n}\left(mol\right)\)
\(M_{MCl_n}=M_M+35,5n=\dfrac{14,799}{\dfrac{0,22}{n}}=\dfrac{14799}{220}n\)(g/mol)
\(\Rightarrow M_M=\dfrac{6989}{220}n\)(MM<90)
Nghiệm duy nhất thỏa n=2, MM=63,54(g/mol)( Cu)
b) Gọi số khối đồng vị X là AX, số khối đồng vị Y là AY
Theo đề và dữ kiện MM=63,54(g/mol). Ta có hệ phương trình:
\(\left\{{}\begin{matrix}A_X+A_Y=128\\M_M=63,54=\dfrac{A_X.0,37+A_Y.1}{0,37+1}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}A_X=65\\A_Y=63\end{matrix}\right.\)