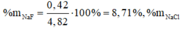Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

KH nguyến tố halogen là X , đặt a là số mol ptu X2
ptpu:
Mg + X2 ----> MgX2
mol : a−−>a
2Al + 3X2 ---> 2AlX3
mol: a−−−>\(\frac{2a}{3}\)
từ pt => (24 + 2X).a =19 => a=\(\frac{19}{24+2X}\)
(27 + 3X).1,5a =17,8 => a= \(\frac{17,8.3}{\left(27+3X\right).2}\) =>X=35,5
![]()

a) Phương trình hóa học của phản ứng: Gọi X là kí hiệu nguyên tử khối của halogen.
Mg + X2 → MgX2
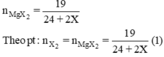
2Al + 3X2 → 2AlX3.
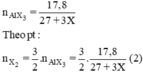
Cho (1) = (2). Giải ta rút ra X = 35,5 (Cl)
b) Thay X = 35,5 vào (1) ⇒ nCl2 = 0,2 mol ⇒ mCl2 = 14,2g.

Mg+X2---->MgX2
n Mg=12/24=0,5(mol)
n MgX2=\(\frac{47,5}{24+2X}\left(mol\right)\)
Theo pthh
n Mg=n MgX2
-->\(\frac{47,5}{24+2X}=0,5\Leftrightarrow47,5=12+X\)
-->X=35,5(Cl)
Vậy .......

Câu 1:
Cho hỗn hợp X vào HCl chỉ có Fe phản ứng:
Fe + 2HCl --> FeCl2 + H2
Ta có: nH2=0,448/22,4=0,02 mol=nFe
Cho X tác dụng với Cl2
2Fe + 3Cl2 --> 2FeCl3
Cu + Cl2 --> CuCl2
-> nFeCl3=nFe=0,02 mol -> mFeCl3=0,02.(56+35,5.3)=3,25 gam
-> mCuCl2=7,3-3,25=4,05 gam -> nCuCl2=4,05/(64+35,5.2)=0,03 mol=nCu
->m=mFe +mCu=0,02.56+0,03.64=3,04 gam
Câu 2:
2Al +6HCl -->2AlCl3 + 3H2
Fe+2HCl--> FeCl2 + H2
27nAl+56nFe=8,3(1)
nH2=5,6/22,4=0,25
3nAl+2nFe=2nH2=0,25.2=0,5(2)
(1)(2)nAl=nFe=0,1
%mAl=0,1.27/8,3 .100=32,53%
%mFe=100-32,53=67,47%
nHCl=2nH2=0,25.2=0,5
nHCl ban đầu =0,5.120%=0,6
VddHCl=0,6/1=0,6lit
Câu 3:
Mg+X2->MgX2
2Al+3X2->2AlX3
nX2=19/24+2MX
nX2=3/2.17,8/27+3MX
=>19/24+2MX=26,7/27+3MX
=>MX=35,5g/mol
=>X:Clo(Cl)
nCl2=nMgCl2=19/95=0,2mol
=>mCl2=0,2.71=14,2g
Câu 4:
H2+Cl2->2HCl
VH2pu=VCl2pu=VHCl/2=0,4/2=0,2l
=>VH2=0,4−0,2=0,2l
=>VCl2=0,6−0,2=0,4mol
%VCl2=0,4/0,4+0,2+0,2.100%=50%
%VH2=%VHCl=25%