Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Al}=\dfrac{3}{27}=\dfrac{1}{9}\left(mol\right)\)
\(n_{HCl}=\dfrac{7.3}{36.5}=0.2\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(TC:\)
\(\dfrac{\dfrac{1}{9}}{2}>\dfrac{0.2}{6}\Rightarrow Aldư\)
\(n_{AlCl_3}=\dfrac{0.2\cdot2}{6}=\dfrac{1}{15}\left(mol\right)\)
\(m=\dfrac{1}{15}\cdot133.5=8.9\left(g\right)\)

nAl = \(\dfrac{1,35}{27}=0,05\) mol
nHCl = \(\dfrac{7,3}{36,5}=0,2\) mol
Pt: 2Al + 6HCl --> 2AlCl3 + 3H2
.....0,05-> 0,15---> 0,05------>0,075 (mol)
Xét tỉ lệ mol giữa Al và HCl:
\(\dfrac{0,05}{2}< \dfrac{0,2}{6}\)
Vậy HCl dư
mAlCl3 = 0,05 . 133,5 = 6,675 (g)
mH2 = 0,075 . 2 = 0,15 (g)
mHCl dư = (0,2 - 0,15) . 36,5 = 1,825 (g)

Ta có: \(C_{\%_{NaOH}}=\dfrac{m_{NaOH}}{400}.100\%=4\%\)
=> \(m_{NaOH}=16\left(g\right)\)
=> \(n_{NaOH}=\dfrac{16}{40}=0,4\left(mol\right)\)
PTHH: HCl + NaOH ---> NaCl + H2O
Theo PT: \(n_{NaCl}=n_{NaOH}=0,4\left(mol\right)\)
=> \(m_{NaCl}=0,4.58,5=23,4\left(g\right)\)

2Al + 6HCl → 2AlCl3 + 3H2
2 6 2 3
0,3 0,9 0,3 0,45
a). nAl= \(\dfrac{8,1}{27}\)=0,3(mol)
⇒ nHCl= \(\dfrac{0,3.3}{6}\)= 0,9(mol).
⇒ mHCl=n.M= 0,9 . 36.5 =32,85(g).
b). nAlCl3= \(\dfrac{0,9.2}{6}\)= 0,3(mol).
⇒mAlCl3= n.M = 0,3 . 133,5 =40,05(g).
c). nH2= \(\dfrac{0,3.3}{2}\)= 0,45(mol).
⇒VH2= n . 22,4 = 0,45 . 22,4= 10,08(g).

HCl+NaOH->NaCl+H2O
0,1---0,1
n NaOH=0,5.0,2=0,1 mol
=>m NaCl=0,1.58,5=5,85g
HCl+NaOH->NaCl+H2O
0,1---0,1
n NaOH=0,5.0,2=0,1 mol
=>m NaCl=0,1.58,5=5,85g

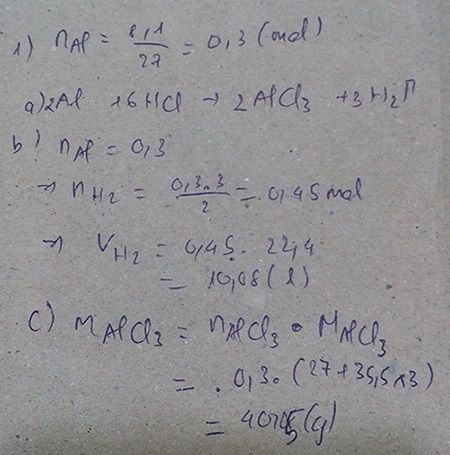
PTHH: 2Al + 6HCl ===> 2AlCl3 + 3H2
Ta có: nAl = \(\frac{1,35}{27}=0,05\left(mol\right)\)
nHCl = \(\frac{7,3}{36,5}=0,2\left(mol\right)\)
Lập tỉ lệ số mol: \(\frac{0,05}{2}< \frac{0,2}{6}\)
=> Al hết, HCl dư
=> Tính theo số mol Al
Theo PTHH, nAlCl3 = nAl = 0,05 (mol)
=> mAlCl3 (tạo thành) = 0,05 x 133,5 = 6,675 (gam)
Ta có:
PTHH: Al + 3HCl -> AlCl3 + \(\frac{3}{2}\)H2
Ta có:
\(n_{HCl}=\frac{7,3}{36,5}=0,2\left(mol\right)\\ n_{Al}=\frac{1,35}{27}=0,05\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(\frac{0,05}{1}=0,05< \frac{0,2}{3}\approx0,067\)
=> Al phản ứng hết, HCl dư nên tính theo nAl.
Theo PTHH và đề bài, ta có:
\(n_{AlCl_3}=n_{Al}=0,05\left(mol\right)\)
Khối lượng AlCl3:
\(m_{AlCl_3}=0,05.133,5=6,675\left(g\right)\)