Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Hướng dẫn giải:
Ta có: nP2O5= 2,13/142= 0,015 mol
P2O5+ 3H2O → 2 H3PO4
0,015 0,03 mol
NaOH + H3PO4 → NaH2PO4 + H2O
2NaOH + H3PO4 → Na2HPO4 + 2H2O
3NaOH + H3PO4 → Na3PO4 + 3H2O
Do trong dung dịch chỉ chứa các muối nên:
Theo các PT ta có: nH2O= nNaOH= V.1/1000= 0,001V (mol)
Áp dụng định luật bảo toàn khối lượng ta có:
mNaOH + mH3PO4= mmuối + mH2O →0,001V. 40 + 0,03.98= 4,48 + 0,001V.18 →V= 70ml

Đáp án C
Đặt nP2O5 = a ⇒ mP2O5 = 142a.
Ta có nH3PO4 = 2nP2O5 = 2a ⇒ nNaOH phản ứng = 6a.
⇒ nNaOH dư = 0,2535 × 2 – 6a = 0,507 – 6a.
+ Vậy từ mối tương quan m và 3m ta có:
3mP2O5 = mNa3PO4 + mNaOH dư.
⇔ 426a = 2a×164 + (0,507 – 6a)×40 ⇔ a = 0,06 mol.
⇔ m = 8,52 gam

Đáp án A
Xét NaOH hết ta có: n H 2 O = n N a O H = 0 , 507 m o l
Bảo toàn khối lượng: m H 3 P O 4 + m N a O H = m c r + m H 2 O
→ 98 71 m + 0 , 507 . 40 = 3 m + 18 . 0 , 507
→ m = 6,89 (g)
Xét NaOH dư ta có:
n H 2 O = 3 n H 3 P O 4 = 3 71 m ( m o l )
Bảo toàn khối lượng:
m H 3 P O 4 + m N a O H = m c r + m H 2 O
→ m = 8,52(g) loại

Đáp án A
![]()
![]()
Xét NaOH hết ta có: n H 2 O = n N a O H = 0 , 507 m o l
Bảo toàn khối lượng: m H 3 P O 4 + m N a O H = m H 2 O + m c r
→ 98 71 m + 0 , 507 . 40 = 3 m + 18 . 0 , 507
→ m = 6,89 (g)
Xét NaOH dư ta có: n H 2 O = 3 n H 3 P O 4 = 3 71 m ( m o l )
Bảo toàn khối lượng:
m H 3 P O 4 + m N a O H = m H 2 O + m c r
→ 98 71 m + 0 , 507 . 40 = 3 m + 18 . 3 71 m
→ m = 8,52(g) loại



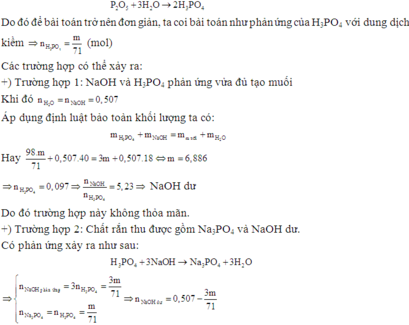
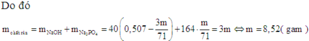
\(\text{nP = mP : MP = 12,4 : 31 = 0,4 (mol)}\)
PTHH:
4P + 5O2 t0\(\underrightarrow{to}\)2P2O5 (1)
0,4_______________ 0,2 (mol)
Theo PTHH (1): nP2O5 = \(\frac{1}{2}\).nP = \(\frac{1}{2}\). 0,4 = 0,2 (mol)
m dd NaOH =80. 1,28=102,4 (g)
mNaOH =\(\text{ 102,4.25%:100% = 25,6 (g)}\)
\(\rightarrow\) nNaOH= mNaOH : M NaOH = \(\text{25,6 : 40 = 0,64 (mol)}\)
Xét P2O5 tác dụng với dd NaOH ta coi như P2O5 tác dụng với H2O tạo ra H3PO4, sau đó H3PO4 mới tác dụng với dd NaOH
PTHH: P2O5 + 3H2O\(\rightarrow\)2H3PO4 (2)
Lập tỉ lệ \(\frac{nNaOH}{nH3PO4}=\frac{0,64}{0,4}=1,6\)
Ta thấy 1 < 1,6 < 2 vậy H3PO4 phản ứng với NaOH cho 2 muối NaH2PO4 và Na2HPO4
PTHH:
H3PO4 + NaOH\(\rightarrow\)NaH2PO4 + H2O (3)
x _________ x________ x__________ (mol)
H3PO4 + 2NaOH\(\rightarrow\) Na2HPO4 + H2O (4)
y ________ 2y_______ y__________ (mol)
Đặt số mol H3PO4 pư ở PT (3) và (4) lần lượt là x và y (mol)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}\Sigma nH3PO4=x+y=0,4\\\Sigma nNaOH=x+2y=0,64\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,16\\y=0,24\end{matrix}\right.\)
Theo PTHH (3): nNaH2PO4 = x = 0,16 (mol)
\(\rightarrow\) mNaH2PO4 = nNaH2PO4. M NaH2PO4 \(\text{= 0,16.120 = 19,2 (g)}\)
Theo PTHH (4): nNa2HPO4 = y = 0,24 (mol)
\(\rightarrow\)mNa2HPO4 = nNa2HPO4.MNa2HPO4 \(\text{= 0,24.142 = 34,08 (g)}\)
dung dịch thu được sau phản ứng là:
mdd sau = mP2O5 + mdd NaOH \(\text{= 0,2.142 + 102,4 = 130,8 (g)}\)
Nồng độ phần trăm của các chất thu được sau phản ứng là:
\(\left\{{}\begin{matrix}C\%NaH2PO4=\frac{19,2}{130,8}.100\%=14,68\%\\C\%Na2HPO4=\frac{34,08}{130,8}.100\%=26,06\%\end{matrix}\right.\)
\(nP_2O_5=\frac{1}{2}nP=\frac{\frac{1}{2}.12,4}{31}=0.2\left(mol\right)\)\(\)
\(nNaOH=\frac{80.1,28.25\%}{40}=0.64\left(mol\right)\)
\(k=\frac{nNaOH}{nP_2O_5}=\frac{0,64}{0,2}< 2=3.2>3\)
=>Tạo 2 muối\(NaH_2PO4,Na_2HPO4\)
Đặt số mol 2 muối lần lượt là x và y,bảo toàn nguyên tố Na và P ta có hệ
\(\left\{{}\begin{matrix}x+2y=0,64\\\frac{1}{2}x+\frac{1}{2}y=0,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,12\\y=0,24\end{matrix}\right.\left(mol\right)\)
C%NaH2PO4=\(\frac{0,12.120}{0,2.112+1,28.80}.100\simeq11,53\%\)
C%NaHPO4=\(\frac{0,24.142}{0.2.112+1.28.80}.100\simeq27,3\%\)
Ở dòng đầu mình bảo toàn nguyên tố P nha,và mdd=mP2O5+mddNaOH,bạn chú ý m dung dịch NaOH=d/V dd