Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nồng độ FeCl2: CM=0,2M thể tích dd: Vdd = 600ml = 0,6lit
 Vậy số mol FeCl2
Vậy số mol FeCl2 
Pt:

 khối lượng
khối lượng
Vậy m là 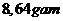

Phương trình: 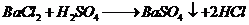
Vậy kết tủa là 

Số mol
Phương trình
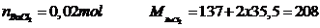

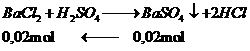
 khối lượng
khối lượng
Vậy m là 

Bạn nên thêm ↑ vào sau chỗ \(H_2\) nhé
Cho Mg và Cu vào HCl thì chỉ có Mg pứ (Cu ko Pứ vì Cu đứng sau H trong dãy điện hóa)
 Thể tích khí H2:
Thể tích khí H2: 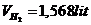
 |
 Số mol
Số mol
Phương trình :



 khối lượng
khối lượng
Vậy khối lượng Mg : 
Vậy khối lượng Cu: 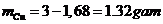
nH2=\(\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
Mg+2HCl\(\rightarrow\)MgCl2+H2
0,07.........................0,07(mol)
Cu+HCl không pứ
\(\Rightarrow\)mMg=0,07.24=1,68(g)
\(\Rightarrow\)mCu=3-1,68=1,32(g)
Chúc bạn học tốt!


Số mol
Phương trình
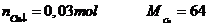
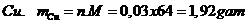
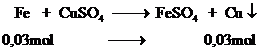
 khối lượng
khối lượng
Vậy khối lượng kim loại  là 1,92 gam
là 1,92 gam

Thể tích khí H2: 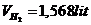

 Số mol
Số mol
Phương trình :



 khối lượng
khối lượng
Vậy khối lượng Mg : 
Vậy khối lượng Cu: 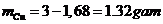

Số mol
Phương trình :

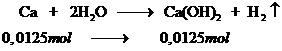
Số mol Ca(OH)2 tạo thành
Thể tích dd :
Nồng độ dd Ca(OH)2


Số mol
Phương trình
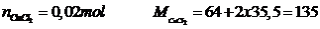
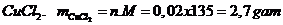
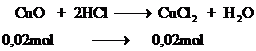
 khối lượng
khối lượng
Vậy khối lượng muối  khan là 2,7 gam
khan là 2,7 gam

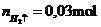
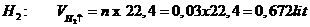



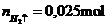

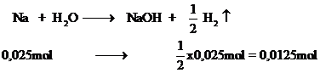


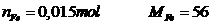


Pt:
Số mol tạo thành
tạo thành
Thể tích dd :
Nồng độ dd
thanks bạn nha