Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Gọi số mol HCl là x mol
HCl + KOH → KCl + H2O
x x (mol)
Giả sử KOH hết ⇒ mKCl = 74,5 . 0,1 = 7.45(g) > 6,525 ⇒KOH dư ,HCl hết.
(0,1 - x).56 + x.(39 + 35,5) = 6,525
⇒ x = 0,05 mol ⇒ CM = 0,5M

2Na + 2HCl → 2NaCl + H2
x---------------------x
2Na + 2H2O → 2NaOH + H2
y----------------------y
Ta có: x + y = 0,2 và 58,5x + 40y = 9,85 → x = y = 0,1 mol → [HCl] = 1M

Đổi 100ml = 0,1l
\(n_{NaOH}=0,1.1=0,1\left(mol\right)\)
\(n_{HCl}=0,1.2=0,2\left(mol\right)\)
PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Theo PT và đề bài ta lập tỉ lệ:
\(\dfrac{0,1}{1}< \dfrac{0,2}{1}\Rightarrow\) HCl dư. NaOH hết => tính theo \(n_{NaOH}\)
Theo PT: \(n_{HCl\left(pư\right)}=n_{NaOH}=0,1\left(mol\right)\)
=> \(n_{HCl\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\)
=> \(CM_{dd_{HCl}}=\dfrac{0,1}{0,1+0,1}=0,5\left(M\right)\)
Theo PT ta có: \(n_{NaOH}=n_{NaCl}=0,1\left(mol\right)\)
=> \(CM_{dd_{NaCl}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)

a, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có: \(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{HCl}=2n_{Fe}=0,5\left(mol\right)\\n_{H_2}=n_{Fe}=0,25\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow V_{H_2}=0,25.24,79=6,1975\left(l\right)\)
\(a=C_{M_{HCl}}=\dfrac{0,5}{0,1}=5\left(M\right)\)
b, Theo PT: \(n_{FeCl_2}=n_{Fe}=0,25\left(mol\right)\)
Ta có: \(n_{AgNO_3}=0,4.1,3=0,52\left(mol\right)\)
PT: \(2AgNO_3+FeCl_2\rightarrow Fe\left(NO_3\right)_2+2AgCl_{\downarrow}\)
______0,5______0,25______0,25________0,5 (mol)
\(AgNO_3+Fe\left(NO_3\right)_2\rightarrow Fe\left(NO_3\right)_3+Ag_{\downarrow}\)
0,02______0,02________0,02________0,02 (mol)
⇒ m = mAgCl + mAg = 0,5.143,5 + 0,02.108 = 73,91 (g)
- Dd sau pư gồm: Fe(NO3)3: 0,02 (mol) và Fe(NO3)2: 0,25 - 0,02 = 0,23 (mol)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{Fe\left(NO_3\right)_3}}=\dfrac{0,02}{0,1+0,4}=0,04\left(M\right)\\C_{M_{Fe\left(NO_3\right)_2}}=\dfrac{0,23}{0,1+0,4}=0,46\left(M\right)\end{matrix}\right.\)
\(Fe+2HCl->FeCl_2+H_2\\ a.V=\dfrac{14}{56}\cdot22,4=5,6\left(L\right)\\ a=\dfrac{\dfrac{14}{56}\cdot2}{0,1}=5\left(M\right)\\ b.n_{AgNO_3}=0,4\cdot1,3=0,52mol\\ FeCl_2+AgNO_3->Fe\left(NO_3\right)_2+AgCl\\ Fe\left(NO_3\right)_2+AgNO_3->Ag+Fe\left(NO_3\right)_3\\ m=0,25\cdot143,5+0,25\cdot108=62,875\left(g\right)\\ C_{M\left(AgNO_3\right)}=\dfrac{0,02}{0,5}=0,04M\\ C_{M\left(Fe\left(NO_3\right)_3\right)}=\dfrac{0,25}{0,5}=0,5M\)

MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
nHCl = \(\dfrac{20.36,5\%}{36,5}\)= 0,2 mol => nCl2 = 0,2 : 4 = 0,05 mol
Cl2 + 2KOH →KCl + KClO + H2O
nKOH = 0,5.2 = 1 mol
=> KOH dư , Cl2 hết
nKOH dư = 1 - 0,05.2 = 0,9 mol
dung dịch A gồm KCl và KClO có số mol = nCl2 = 0,05 mol và KOH dư 0,9mol
CKCl = CKClO = \(\dfrac{0,05}{0,5}\)=0,1 M
CKOH dư = \(\dfrac{0,9}{0,5}\)= 1,8 M

Đáp án A
nKOH = 0,1.1=0,1 (mol)
KOH + HCl →KCl + H2O
0,1→ 0,1 (mol)
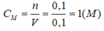
Giả sử HCl hết, KOH dư,\(CM_{KOH}=1M\)
\(KOH+HCl\rightarrow KCl+H_2O\)
Gọi a là số mol của KOH phản ứng
\(n_{KOH\left(dư\right)}=0,1-a\)
Chất tan sau phản ứng gồm: KCl a (mol) và KOH dư 0,1-a (mol)
\(74,5a+56.\left(0,1-a\right)=11,1\)
\(\Rightarrow a=0,3\left(mol\right)\)
\(CM_{HCl}=\frac{0,3}{0,1+0,1}=1,5M\)
HCl dư, KOH hết
Gọi a là số mol của HCl phản ứng
\(n_{HCl\left(dư\right)}=0,1-a\)
\(56a+74,5.\left(0,1-a\right)=11,1\)
\(\Rightarrow a=-0,2\)
Vậy giả sử 1 đúng