Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Zn + 2HCl → ZnCl2 + H2
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
b) Theo PT: \(n_{Zn}pư=n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Zn}pư=0,2\times65=13\left(g\right)\)
c) Theo PT: \(n_{ZnCl_2}=n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow C_{M_{ZnCl_2}}=\dfrac{0,2}{0,07}=2,9\left(M\right)\)
Zn + 2HCl -> ZnCl2 + H2
Ta có:
nH2 = 4,48/22,4 = 0,2 mol
Theo pthh và bài ta có:
+ nZn = nH2 = 0,2 mol
=>mZn = 0,2 . 65 = 13 g
+ nZnCl2 = nH2 = 0,2 mol
=>CM dd ZnCl2 = 0,2 / 0,07 = 2,9 M
Vậy...

a, Zn + 2HCl--> ZnCl2 + H2
b , Ta có nH2=4,48/22,4=0,2 mol
Ta có nZn PỨ = nH2= 0,2 mol
=> mZn PỨ= 0,2.65=13 g
c, Ta có nMgCl2=mH2=0,2 mol
=> CM dd MgCl2=0,2/0,07=2,857 M

a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,3.65=19,5\left(g\right)\)
c, \(n_{HCl}=2n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,1}=6\left(M\right)\)

\(n_{H_2}=\dfrac{2,479}{22,4}=\dfrac{2479}{22400}mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo pt ta có: \(n_{Zn}=n_{H_2}=\dfrac{2479}{22400}mol\)\(\approx0,11mol\)
\(\Rightarrow m_{Zn}\approx7,2g\)
\(n_{HCl}=2n_{H_2}=0,22mol\) \(\Rightarrow C_{M_{HCl}}=\dfrac{0,22}{0,1}=2,2M\)

Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
a) Pt : 2Al +6HCl → 2AlCl3 + 3H2\(|\)
2 6 2 3
0,5 1,5 0,75
a) Số mol của nhôm
nAl = \(\dfrac{0,75.2}{3}=0,5\left(mol\right)\)
Khối lượng của nhôm
mAl = nAl . MAl
= 0,5 .27
= 13,5 (g)
c) Số mol của dung dịch axit clohidric
nHCl = \(\dfrac{0,5.6}{2}=1,5\left(mol\right)\)
500ml = 0,5l
Nồng độ mol của dung dịch axit clohdric đã dùng
CMHCl = \(\dfrac{n}{V}=\dfrac{1,5}{0,5}=3\left(M\right)\)
Chúc bạn học tốt
2Al+6HCl->2AlCL3+3H2
=>nAl=\(\dfrac{2}{3}\)nH2=\(\dfrac{2}{3}\).16,8/22.4=0,5mol
=>mAl=27.0,5=13,5g
=>nHCl=2nH2=2.16,8/22,4=1,5mol
\(=>Cm=\dfrac{1,5}{\dfrac{500}{1000}}=3M\)

nH2=0,15mol
PTHH: Fe+2HCL=>FeCl2+H2
0,15<-0,3<-0,15<-0,15
mFe tham gia phản ứng :
mFe=0,15.56=8,4g
CM (HCl)=n:V=0,3:0,05=6M
n(H2)=3,36/22,4=0,15
Fe + 2HCl--->FeCl2+H2
0,15....0,3.....................0,15
m(Fe) t/g p/u=0,15*56=8,4(g)
Cm(HCl)=0,3/(50/1000)=6 M

a) PTHH: Zn + H2SO4 -> ZnSO4 + H2
nH2= 0,15(mol)
=> nZn=nH2SO4=nZnSO4=nH2=0,15(mol)
b) mZn=0,15.65=9,75(g)
c) CMddH2SO4= 0,15/ 0,05=3(M)
d) mZnSO4= 161. 0,15=24,15(g)
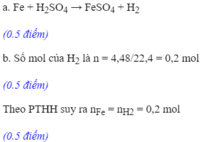

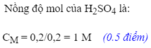
a) Zn + 2HCl \(\rightarrow\) ZnCl2 + H2\(\uparrow\)
b) \(n_{H_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo phương trình: \(n_{Zn}=1\) ; \(n_{H_2}=1\) ; \(n_{HCl}=2\)
Mà \(n_{H_2}=0,2\left(mol\right)\Rightarrow n_{Zn}=0,2\left(mol\right)\) ; \(n_{HCl}=0,4\left(mol\right)\)
Ta có: \(m_{Zn}=n_{Zn}.M_{Zn}=0,2.65=13\left(g\right)\)
c) Đổi: 70ml = 0,07l
\(C_M=\dfrac{n}{V}=\dfrac{0,4}{0,07}\approx5,7\left(M\right)\)
đúng ko v bạn