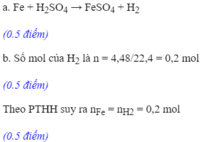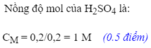Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{V_{H_2}}{22,4}=\dfrac{3,36}{22,4}=0,15mol\)
a. PTHH: Fe + H2SO4 \(\rightarrow\) FeSO4 + H2
TL: 1 1 1 1
mol: 0,15 \(\leftarrow\) 0,15 \(\leftarrow\) 0,15 \(\leftarrow\) 0,15
\(b.m_{Fe}=n.M=0,15.56=8,4g\)
Đổi 150ml = 0,15 l
\(c.C_{MddH_2SO_4}=\dfrac{n}{V}=\dfrac{0,15}{0,15}=1M\)

Bài 2 :
a) Theo đề bài ta có : nH2SO4(điều chế được) = 4.5 = 20 (mol)
=> mddH2SO4(cần) = \(\dfrac{20.98.100\%}{98\%}=2000\left(g\right)\)
=> VddH2SO4(cần) = \(\dfrac{2000}{1,84}\approx1087\left(ml\right)\)
Bài 3 :
Theo đề bài ta có : nH2 = \(\dfrac{33,6}{22,4}=1,5\left(mol\right)\)
Ta có PTHH :
\(Fe+H2SO4->FeSO4+H2\uparrow\)
1,5mol....1,5mol........1,5mol......1,5mol
a) Ta có : mFe = 1,5.56 = 84(g)
b) Ta có : nFeSO4 = nFeSO4.7H2O = 1,5 (mol)
=> mFeSO4.7H2O = 1,5. 278 = 417(g)
c) Ta có : CMH2SO4 = \(\dfrac{1,5}{0,5}=3\left(M\right)\)
Vậy................

a) PTHH: Fe + H2SO4 => FeSO4 + H2
....Số mol của H2 là:
.......nH2 = V : 22,4 = 33,6l : 22,4 = 1,5mol
....Số mol của Fe là:
.......nFe = nH2 = 1,5mol
....Vậy khối lượng của Fe là:
.......mFe = n . M = 1,5mol . 56g = 84g
b) PTHH: FeSO4.7H2O => FeSO4 + 7H2O
....Số mol của FeSO4 là:
.......nFeSO4 = nH2 = 1,5mol
....Vậy khối lượng của FeSO4 là:
.......mFeSO4 = n . M = 1,5mol . 152g = 228g
....Biết khối lượng mol FeSO4.7H2O = 278g
..................//..............FeSO... = 152g
...........khối lượng của FeSO4 = 228g
....Gọi khối lượng của FeSO4.7H2O là a
....Ta có tỷ lệ:
.......(278g : a) = (152g : 228g) <=> 278g : x = 2/3
......................................... a = 417g
c) Số mol của H2SO4 là:
.......nH2SO4 = nH2 = 1,5mol
....Đổi 500ml = 0,5l
....Nồng độ mol của H2SO4 là:
.......CMH2SO4 = n : V = 1,5mol : 0,5l = 3M
....Đáp số:
.............a) mFe = 84g
.............b) a (mFeSO4.7H2O) = 417g
.............c) CMH2SO4 = 3M
a>Fe+H2SO4 =FeSO4 +H2
nFe(phản ứng)=nH2=33,6/22,4=1,5mol -->mFe(pứ)=1,5.56=84 g
b>vì nFeSO4=nFeSO4.7H2O
nên a=mFeSO4.7H2O=1,5.(152+7.18)=417g
c>nH2SO4=nH2=1,5 mol -->MddH2SO4=1,5/0,5=3M

a) Fe + H2SO4 -----------> FeSO4 + H2
\(n_{Fe}=n_{H_2}=0,75\left(mol\right)\)
=> \(m_{Fe}=0,75.56=42\left(g\right)\)
b) \(CM_{H_2SO_4}=\dfrac{0,75}{0,25}=3M\)
c) \(m_{ddsaupu}=42+250.1,1-0,75.2=315,5\left(g\right)\)
=> \(C\%_{FeSO_4}=\dfrac{0,75.152}{315,5}.100=36,13\%\)
\(n_{SO_2}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
\(PTHH:2Fe+6H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
Mol: 0,5 1,5 0,25 0,75 1,5
a)mFe=0,5.56=28 (g)
b)\(C_{MddH_2SO_4}=\dfrac{1,5}{0,25}=6\left(mol/l\right)\)
c)\(m_{Fe_2\left(SO_4\right)_3}=0,25.400=100\left(g\right)\)
\(m_{H_2O}=1,5.18=27\left(g\right)\)
\(C\%_{ddFe_2\left(SO_4\right)_3}=\dfrac{100.100}{100+27}=78,74\%\)

Na2CO3 + H2SO4 -> Na2SO4 + CO2 + H2O
CO2 + 2NaOH -> Na2CO3 + H2O
a 2a a
CO2 + NaOH -> NaHCO3
b b b
nNaOH= \(\frac{8\cdot40\%}{40}\)= 0,08 mol
Theo đề bài ta có hệ pt
2a+b=0,08
106a+84b= 5,48
=> a=0,02 b=0,04
%mNa2CO3 = \(\frac{0,02\cdot106}{5,48}\)*100% = 38,69%
%mNaHCO3 = 61,31%
nCO2 = 0,02+0,04=0,06
CMH2SO4 = 0,06/0,2=0,3 M

Bài 2
Gọi x, y là số mol củaCuO và ZnOmol HCl=3.0,1=0,3mol(100ml=0,1l)
CuO+2HCl->CuCl2+H2O (1)
xmol 2xmol
ZnO+2HCl->ZnCl2+H2O(2)
ymol 2ymol
Từ 1 và 2 ta co hệ phương trình
2x+2y=0,3 ->x=0,05=molCuO
80x+81y=12,1 ->y=0,1=molZnO
=>mCuO=0,05.80=4g
->%CuO=(4.100)/12,1=33,075%
->%ZnO=100-33,075=66,943%
b. CuO+H2SO4->CuSO4+H2O (3)
Theo ptpu 3 taco nH2SO4=nCuO=0,05 mol
ZnO+H2SO4->ZnSO4+H2O (4)
Theo ptpu 4 ta co nH2SO4=nZnO=0,1mol
=>nH2SO4=0.05+0,1=0,15mol
->mH2SO4=0,15.98=14,7g
=>mddH2SO4=(14,7.100)/20=73,5g
Bài 1
a/. Phương trình phản ứng hoá học:
Fe + 2HCl --> FeCl2 + H2
b/. nH2 = V/22,4 = 3,36/22,4 = 0,15 (mol)
....... Fe.....+ 2HCl --> Fecl2 + H2
TPT 1 mol....2 mol.................1 mol
TDB x mol....y mol................0,15 mol
nFe = x = (0,15x1)/1 = 0,15 (mol)
mFe = n x M = 0,15 x 56 = 8,4 (g)
c/. nHCl = y = (0,15x2)/1 = 0,3 (mol)
CMHCl = n/V = 0,3/0,05 = 6 (M)

15
a)\(Fe+H2SO4-->FeSO4+H2\)
\(n_{H2}=\frac{33,6}{22,4}=1,5\left(mol\right)\)
\(n_{Fe}=n_{H2}=1,5\left(mol\right)\)
\(m_{Fe}=1,5.56=84\left(g\right)\)
b)\(n_{FeSO4}=n_{H2}=1,5\left(mol\right)\)
\(m=m_{FeSO4}=1,5.152=228\left(g\right)\)
c)\(n_{H2SO4}=n_{H2}=1,5\left(mol\right)\)
\(C_{M\left(H2SO4\right)}=\frac{1,5}{0,5}=3\left(M\right)\)
16.
n\(_{H2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
Gọi \(n_{Mg}=x,n_{Fe}=y\)
\(Mg+2HCl--.MgCl2+H2\)
x-------------------------x----------x(mol)
\(Fe=2HCl-->FeCl2+H2\)
y----------------------------y------y(mol)
Theo bài ta có hpt
\(\left\{{}\begin{matrix}24x+56y=4\\x+y=0,1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
\(m_{MgCl2}=0,05.95=4,75\left(g\right)\)
\(m_{FeCl2}=0,05.127=6,35\left(g\right)\)
17.
\(n_{H2}=\frac{13,44}{22,4}=0,6\left(mol\right)\)
\(Fe+2HCl--.FeCl2+H2\)
x----------------------------------x(mol)
\(2Al+6HCl--.2AlCl3+3H2\)
y----------------------------------------1,5y(mol)
theo bài ta có hpt
\(\left\{{}\begin{matrix}56x+27y=22,2\\x+1,5y=0,6\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\)
\(\%m_{Fe}=\frac{0,3.56}{22,2}.100\%=75,68\%\%\)
\(\%m_{Al}=100-75,68=24,32\%\)
18.
\(Mg+2HCl--.MgCl2+H2\)
\(Fe+2HCl--.FeCl2+H2\)
Chất rắn k tan là Cu = 2,54(g)
=>\(m_{Mg+Fe}=10,54-02,54=10\left(g\right)\)
\(n_{H2}=\frac{4,48}{22,4}=0,2\left(mol\right)\Rightarrow m_{H2}=0,4\left(g\right)\)
\(n_{HCl}=n_{H2}=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(m=m_{Fe+Mg}+m_{HCl}-m_{H2}=10+14,6-0,4=24,2\left(g\right)\)