Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

đề cho có bị sai số liệu không?
Thể tích khí Cl2 sao lại là 13,32(l) ????

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

a) Đặt \(\hept{\begin{cases}n_{Al}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{cases}}\)
PTHH : \(2Al+3H_2SO_4-->Al_2\left(SO_4\right)_3+3H_2\) (1)
\(Al+6HNO_3-->Al\left(NO_3\right)_3+3NO_2+3H_2O\) (2)
\(Cu+4HNO_3-->Cu\left(NO_3\right)_2+2NO_2+2H_2O\) (3)
Theo pthh (1) : \(n_{Al}=\frac{2}{3}n_{H_2}=0,2\left(mol\right)\) => \(x=0,2\left(mol\right)\)
Theo ptr (2); (3) : \(n_{NO_2}=3n_{Al}+2n_{Cu}\)
=> \(0,8=0,2\cdot3+2\cdot n_{Cu}\)
=> \(n_{Cu}=0,1\left(mol\right)\)
=> \(a=0,2\cdot27+0,1\cdot64=11,8\left(g\right)\)
b) PTHH : \(NH_3+HNO_3-->NH_4NO_3\) (4)
\(3NH_3+3H_2O+Al\left(NO_3\right)_3-->Al\left(OH\right)_3\downarrow+3NH_4NO_3\) (5)
\(2NH_3+2H_2O+Cu\left(NO_3\right)_2-->Cu\left(OH\right)_2\downarrow+2NH_4NO_3\) (6)
BT Al : \(n_{Al\left(OH\right)_3}=n_{Al}=0,2\left(mol\right)\)
BT Cu : \(n_{Cu\left(OH\right)_2}=n_{Cu}=0,1\left(mol\right)\)
=> \(m\downarrow=m_{Al\left(OH\right)_3}+m_{Cu\left(OH\right)_2}=25,4\left(g\right)\)
c) Gọi tên KL là X .
PTHH : \(2Al\left(NO_3\right)_3-t^o->Al_2O_3+6NO_2+\frac{3}{2}O_2\) (7)
\(Cu\left(NO_3\right)_2-t^o->CuO+2NO_2+\frac{1}{2}O_2\) (8)
\(4NO_2+O_2+2H_2O-->4HNO_3\) (9)
\(3X+4nHNO_3-->3X\left(NO_3\right)_n+nNO+2nH_2O\) (10)
viết ptr rồi, nhưng mik có thắc mắc là cho khí B hấp thụ vô nước => tính đc số mol của hno3, rồi áp vô X là ra, nhưng đề lại cho số mol NO =((( hoặc có thể dùng số mol NO để tính nhưng như thế có hơi thừa ko ? tính ra theo 2 cách thì cx ra 2 kq khác nhau ? ai githich giùm mik, hay mik tính sai hoặc phân tích đề sai nhỉ ?? :D

Cho 16,2 gam kim loại M có hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hòa tan vào dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). Kim loại M là
A. Fe
B. Al
C. Ca
D. Mg

Gọi hóa trị của M là n
Gọi nMg = x mol ⇒ nFe = 3.x mol
Số mol H2 là: nH2 = 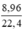 = 0,4 (mol)
= 0,4 (mol)
Số mol Cl2 là: nCl2 = 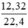 = 0,55 (mol)
= 0,55 (mol)
Các PTHH
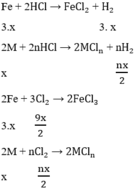
Theo bài ra ta có hệ phương trình:
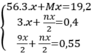
Giải hệ pt ⇒ x = 0,1 mol ⇒ n = 2 ⇒ M = 24
Vậy M là Mg
nMg = 0,1 mol ⇒ nFe = 0,3 mol
Thành phần % theo khối lượng
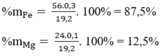

gọi công thức muối là ACO3
n CO2=0,448:22,4=0,02mol
PTHH: ACO3+2HCl=>ACl2+CO2+H2O
0,02<--0,04<-0,02<-0,02->0,02
=> mHCl=0,04.36,5=1,46g
=> mddHCl=\(\frac{1,46}{10}.100=14,6g\)
ta có MACO3=2:0,02=100g/mol
=> M A=100-12-16.3=40
=> A là Ca
=> công thức muois là CACO3
ta có m CaCl2=0,02.111=2,22g
=> mddCaCl2=2+14,6-0,02.44-0,02.18=15,36g
=> C% CaCl2=2,22:15,36.100=14,45%

nH2=0,45 mol
PTHH : 2 M + 2x HCl -->2 MClx + xH2
mol 0,9/x 0,45
mX = 0,9/x *M = 25,2 g
=> M=28x
lập bảng tính được M=56 , x=2
vậy M là Sắt ( Fe)
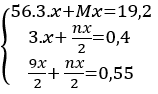
 với các chất sau:
với các chất sau:
\(n_{H_2}=0,336:22,4=0,015mol\)
2M+nHCl\(\rightarrow\)MCln+nH2
\(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,03}{n}mol\)
\(n_{HCl}=0,1mol\)
M=\(\dfrac{0,975n}{0,03}=32,5n\)
n=1\(\rightarrow\)M=32,5(loại)
n=2\(\rightarrow\)M=65(Zn)
n=3\(\rightarrow\)M=97,5(loại)
\(n_{Zn}=\dfrac{0,975}{65}=0,015mol\)
nHCldư=0,1-0,03=0,07mol
\(C_{M_{ZnCl_2}}=\dfrac{0,015}{0,2}=0,075M\)
\(C_{M_{HCl}}=\dfrac{0,07}{0,2}=0,35M\)