Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D.
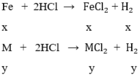
gọi x, y lần lượt là số mol của Fe và M trong hỗn hợp
số mol H2 là 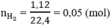
theo bài ra ta có hệ phương trình
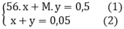
từ (2) → x= 0,05 – y
thay vào (1) ta được 56(0,05 – y) + My = 0,5
⇔ 2,8 – 56y + My = 0,5
2,3 = 56y – My
→ y = 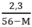
Ta có 0 < y < 0,05
y > 0 ↔ 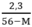 > 0 → 56 – M > 0 ⇒ M < 56
> 0 → 56 – M > 0 ⇒ M < 56
y < 0,05 ↔ 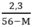 < 0,05 → 2,3 < 0,05(56 – M) → M < 10
< 0,05 → 2,3 < 0,05(56 – M) → M < 10
Trong các kim loại hóa trị II chỉ có Be thỏa mãn do đó M là Be

Đáp án B.
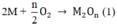
Chất rắn sau phản ứng hòa tan trong HCl thấy có khí thoát ra chứng ở có M dư
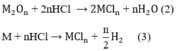
Số mol H2: 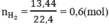
Theo phương trình (1)
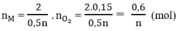
Theo phương trình (3)
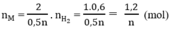
Tổng số mol M là 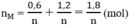
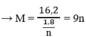
⇒ Giá trị thỏa mãn là n = 3, M = 27 M : Al

Giải thích: Đáp án C
Khi điện phân AgNO3 :
Catot : Ag+ + 1e -> Ag
Anot : 2H2O -> 4H+ + 4e + O2
- Mg + X thu được hỗn hợp kim loại => Ag+ dư
- Hỗn hợp kim loại + HCl => nMg = nH2 = 0,005 mol => nAg = 0,002 mol
Hỗn hợp khí là sản phẩm khử của Mg với H+ và NO3- (Mg dư)
nNO + nN2O = 0,005 mol
mNO + mN2O = 2.19,2.0,005 = 0,192g
=> nNO = 0,002 ; nN2O = 0,003 mol
Gọi nNH4NO3 = x mol
Bảo toàn e : nMg(NO3)2 = nMg + HNO3 + nMg + Ag+ = ½ (3nNO + 8nN2O + 8nNH4NO3) + ½ nAg
= ½ (3.0,002 + 8.0,003 + 8x) + ½ .0,002 = 0,016 + 4x
=> mmuối = mMg(NO3)2 + mNH4NO3 = 148(0,016 + 4x) + 80x = 3,04g
=> x = 0,001 mol
=> nH+(X) = 4nNO + 10nN2O + 10nNH4NO3 = 0,048 mol = ne
Định luật Faraday : ne.F = It => t = 2316 (s)

Giải thích: Đáp án C
(*) Phương pháp : Bảo toàn khối lượng
- Lời giải :
TQ : CO3 + 2HCl → 2Cl + CO2 + H2O
Mol 0,09 ¬ 0,045 0,045
Bảo toàn khối lượng : mCacbonat + mHCl = mMuối Clorua + mCO2 + mH2O
=> m = 21,495g


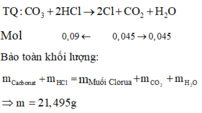
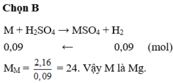
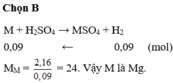
Giải thích: Đáp án C
Gọi kim loại hóa trị II là M
M + 2HCl -> MCl2 + H2
Mol 0,0125 <- 0,0125
=> MM = 40g => Ca