Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

P1: Gọi số mol CO, H2 trong phần 1 là a, b mol
PTHH: CuO + CO --to--> Cu + CO2
CuO + H2 --to--> Cu + H2O
\(n_{Cu}=\dfrac{4,48}{64}=0,07\left(mol\right)\)
=> a + b = 0,07 (1)
P2: Gọi số mol CO, H2 trong phần 2 là ak, bk mol
=> 28ak + 2bk - 28a - 2b = 1,32 (2)
\(n_{CaCO_3}=\dfrac{6}{100}=0,06\left(mol\right)\)
PTHH: CO + O2 --to--> CO2
CO2 + Ca(OH)2 --> CaCO3 + H2O
=> ak = 0,06 (mol) (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,02\\b=0,05\\k=3\end{matrix}\right.\)
=> m = (0,02.28 + 0,05.2) + (0,06.28+0,15.2) = 2,64(g)
\(\left\{{}\begin{matrix}\%CO=\dfrac{0,02}{0,07}.100\%=28,57\%\\\%H_2=\dfrac{0,05}{0,07}.100\%=71,43\%\end{matrix}\right.\)

m rắn giảm = mO (oxit) => nO (oxit) = (1,6 – 1,408) : 16 = 0,012mol
Dễ thấy n = nO (oxit) = 0,012mol
=> nH2 ban đầu = 0,012 : 80% = 0,015
=> nFe = nH2= 0,015 → x = 0,015
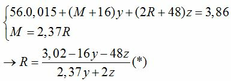
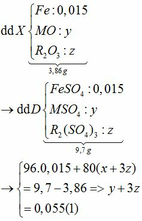
Ta có: CO + O(Oxit) → CO2
Vì: m(Rắn giảm) = mO(Oxit) → nO(Oxit) = (3,86 – 3,46) : 16 = 0,025
TH1: cả 2 oxit đều bị khử bởi CO
→ nO(Oxit) = y + 3z = 0,025 kết hợp với (1) loại
TH2: chỉ có MO bị khử bởi CO
→ nO(Oxit) = nMO = 0,025 → y = 0,025 kết hợp với (1) => z = 0,01
Kết hợp với (*) => M = 64 (Cu)
TH3: chỉ có R2O3 bị khử bởi CO
→ nO(Oxit) = 3.nR2O3 → z = 0,025/3 kết hợp với (1) => y = 0,03
Kết hợp với (*) y => M lẻ => loại
Vậy %m các chất trong X là: 21,76%; 51,81%; 26,43%

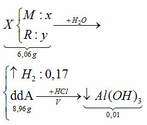
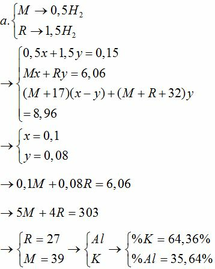
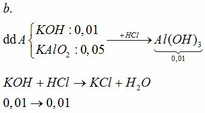
TH1: kết tủa Al(OH)3 chưa bị hòa tan
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,01 ←0,01
→ nHCl = 0,02
→ V = 0,02 (lít) = 20 (ml)
TH2: kết tủa Al(OH)3 bị hòa tan một phần
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,05 → 0,05 0,05
Al(OH)3 + 3HCl → AlCl3 + 3H2O
0,04` → 0,12
→ nHCl = 0,18 → V = 0,18 (l) = 180 (ml)
Vậy có 2 giá trị của V thỏa mãn là: 20 ml và 180 ml

2H(Axit) + O(Oxit) → H2O
→ nH(Axit) = 2.nO(Oxit)
Gọi số mol của Fe3O4 và CuO lần lượt là x và y
BTNT O: 4x + y = 0,6
BTKL: 56 . 3x + 64y = 29,6
=> x = 0,1 và y = 0,2
=> %Fe3O4 = 59,18%
%CuO = 40,82%

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

Phản ứng nhiệt nhôm:
2 A l + F e 2 O 3 → t 0 A l 2 O 3 + 2 F e ( 1 )
Phần 1 tác dụng với dung dịch NaOH dư không sinh ra khí → hỗn hợp B không có Al dư. Vậy hỗn hợp B gồm A l 2 O 3 , Fe và có thể có F e 2 O 3 dư.
4,4 gam chất rắn không tan có thể gồm Fe và F e 2 O 3 d ư
Phần 2: tác dụng với H 2 S O 4 loãng dư → chỉ có Fe phản ứng sinh ra khí
n H 2 = 1,12 22,4 = 0,05
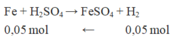
Khối lượng F e 2 O 3 dư ở phần 2 = 4,4 – mFe = 4,4 – 0,05.56 = 1,6 gam.
n F e 2 O 3 p u b d đ = 2. 1 2 . n F e ( p 2 ) = 0,05 m o l
Khối lượng F e 2 O 3 ban đầu: 0,05.160 + 1,6.2 = 11,2 gam.
⇒ Chọn B.
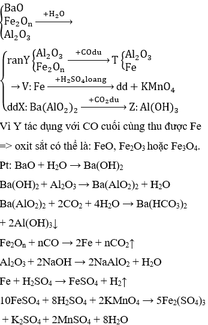

Phần 1 : CuO + CO --to--> Cu + CO2
Al2O3 + 2NaOH ----> 2NaAlO2 + H2O
CR không tan là Cu => nCu(1) = 1,6/64 = 0,025 (mol)
Đặt nAl2O3(1) = a (mol)
=> 0,025.80 + 102a = 2 + 102a = mp1
Phần 2 : Đặt mp2 = kmp1 => mp2 = 2k + 102ka
=> 35,5 = mp1 + mp2 = (k+1)(2 + 102a) (1)
CuO + 2HCl ----> CuCl2 + H2O
0,025k --> 0,05k ---> 0,025k (mol)
Al2O3 + 6HCl ----> 2AlCl3 + 3H2O
ka --->6ka--------> 2ka (mol)
=> 0,025k.135 + 2ka.133,5 = 3,375k + 267ka = 66,9 (2)
Từ (2) => \(k=\dfrac{66,9}{3,375+267a}\), thay vào (1) ta được :
35,5 = \(\left(\dfrac{66,9}{3,375+267a}+1\right)\left(2+102a\right)\)
=> a = 0,05 => k = 4
=> mCuO(A) = 2 + 2.4 = 10 (g)
mAl2O3(A) = 35,5 - 10 = 25,5 (g)
nHCl = 0,05k + 6ka = 0,05.4 + 6.4.0,05 = 1,4
=> VHCl = n/CM = 1,4/2 = 0,7 (l)