Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi kim loại cần tìm là A
a) PTHH: \(A+H_2O\rightarrow AOH+\dfrac{1}{2}H_2\uparrow\)
\(AOH+HCl\rightarrow ACl+H_2O\)
b) Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) \(\Rightarrow n_A=0,2mol\)
\(\Rightarrow M_A=\dfrac{7,8}{0,2}=39\) \(\Rightarrow\) Kim loại cần tìm là Kali
b) Ta có: \(\left\{{}\begin{matrix}n_{KCl}=0,2mol\\n_{HCl\left(pư\right)}=0,2mol\Rightarrow n_{HCl\left(dư\right)}=0,2\cdot20\%=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{KCl}=0,2\cdot74,5=14,9\left(g\right)\\m_{HCl\left(dư\right)}=0,04\cdot36,5=1,46\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{H_2}=2\cdot0,1=0,2\left(g\right)\)
\(\Rightarrow m_{dd}=m_K+m_{ddHCl}-m_{H_2}=7,8+\dfrac{0,24\cdot36,5}{10\%}-0,2=95,2\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{KCl}=\dfrac{14,9}{95,2}\cdot100\%\approx15,65\%\\C\%_{HCl\left(dư\right)}=\dfrac{1,46}{95,2}\cdot100\%\approx1,53\%\end{matrix}\right.\)

Vì hợp chất với hidro có dạng RH => X hoặc Y thuộc nhóm IA hoặc VIIA
*TH1: Y thuộc nhóm IA => CT hidroxit : YOH
theo đề ta có: Y/(Y+17)=0.35323
=>Y=9.28 (loại)
*TH2: Y thuộc nhóm VIIA=> CT hidroxit: HYO4
theo đề ta có: Y/(1+Y+16.4)=0.35323
=> Y=35.5 Cl
theo đề ta thấy: trung hòa A cần dùng dung dịch B. Mà B là axit => A là bazo
=> X thuộc nhóm IA => CTHH: XOH
PT: XOH + HClO4 -> XClO4 +H2O
0.15 0.15 (MOL)
m(XOH)=(50.16,8)/100=8,4=>M(XOH)=m/n=56=>X=39 (Kali)
Hợp chất với hiđro có dạng RH nên Y có thể thuộc nhóm IA hoặc VIIA.
Trường hợp 1 : Nếu Y thuộc nhóm IA thì B có dạng YOH
Ta có : \(\frac{Y}{17}=\frac{35,323}{64,677}\Rightarrow\)\(Y=9,284\) (loại do không có nghiệm thích hợp)
Trường hợp 2 : Y thuộc nhóm VIIA thì B có dạng HYO4
Ta có : \(\frac{Y}{65}=\frac{35,323}{64,377}\Rightarrow Y=35,5\), vậy Y là nguyên tố clo (Cl).
B (HClO4) là một axit, nên A là một bazơ dạng XOH
\(m_A=\frac{16,8}{100}.50g=8,4g\)
XOH + HClO4 \(\rightarrow\) XClO4 + H2O
\(\Rightarrow n_A=n_{HClO_4}=0,15L.0,1\text{/}L=0,15mol\)
\(\Rightarrow M_X+17g\text{/}mol=\frac{0,84g}{0,15mol}\)
\(\Rightarrow\) MX = 39 gam/mol, vậy X là nguyên tố kali (K).

Câu 1:
Hợp chất KHí với Hidro: RH2
\(\Rightarrow\) Ngtố ∈ nhóm VIA \(\Rightarrow\) Oxit cao nhất: RO3
%O = 60% \(\Rightarrow\)%R = 40%
\(\Rightarrow\)\(\dfrac{\%R}{\%O}\)=\(\dfrac{1.M_R}{3.M_O}\)\(\Rightarrow\)\(\dfrac{\text{40%}}{60\%}\)=\(\dfrac{M_R}{3.16}\)\(\Rightarrow\)MR= 32 g/mol
\(\Rightarrow\)Ngtố S
b) Ta có C% =\(\dfrac{m_{ct}}{m_{dd}}\).100 \(\Rightarrow\)mct=\(\dfrac{C\%.m_{dd}}{100}\)= \(\dfrac{19,6.100}{100}\)=19,6 g
Mà mdd= mct + mdung môi \(\Rightarrow\)mdung môi=mdd - mct = 100 - 19,6 = 80,4g
Câu 2 THÌ MÌNH LƯỜI QUÁ :))

Vì R là 1 KL thuộc nhóm IIIA
\(\Rightarrow CTHH:R_2O_3\)
Có \(\frac{2R}{2R+16\times3}=\frac{52,94}{100}\Rightarrow R\approx27\left(Al\right)\)
R là Nhôm . KHHH là Al có NTK là 27
\(n_{Al_2O_3}=\frac{20,4}{2\times27+16\times3}=0,2\left(mol\right)\)
Gọi CTHH là : HX (Vì X thuộc VIIA nên x với H tạo khí hóa trị I)
PTHH
\(Al_2O_3+6HX\rightarrow2AlX_3+3H_2O\)
Theo PTHH có \(n_{HX}=6n_{Al_2O_3}=1,2\left(mol\right)\)
Lại có \(m_{HX}=\frac{18,25\times240}{100}=43,8\left(g\right)\)
\(\Rightarrow M_{HX}=\frac{43,8}{1,2}=36,5\Leftrightarrow1+X=36,5\Leftrightarrow X=35,5\left(Cl\right)\)
Vậy dd B là \(AlCl_3\)
Theo PTHH \(n_{AlCl_3}=2n_{Al_2O_3}=0,4\left(mol\right)\Rightarrow m_{AlCl_3}=0,4\times133,5=53,4\left(g\right)\)
\(m_{ddsaupu}=20,4+240=260,4\left(g\right)\)
\(\Rightarrow C\%\left(AlCl_3\right)=\frac{53,4}{260,4}\times100\approx20,51\%\)

Câu 3. Hòa tan 13,7 gam Ba trong 250ml H2O (D = 1,008 g/ml) thu được dung dịch X và khí Y (đktc)
a) Tính C% của dung dịch X.
b) Lấy 212,4 gam dung dịch X tác dụng với 14,7 gam dung dịch H2SO440% thu được dung dịch Z. Tìm C% các chất tan trong Z.
Giải :
\(a)n_{Ba}=\dfrac{13,7}{137}=0,1\left(mol\right)\\ Ba+H_2O\rightarrow Ba\left(OH\right)_2+H_2\\ n_{Ba\left(OH\right)_2}=n_{H_2}=n_{Ba}=0,1\left(mol\right)\\m_{H_2}=0,1.2=0,2\left(g\right)\\ m_{H_2O}=250.1,008=252\left(g\right)\\ m_{ddsaupu}=13,7+252-0,2=265,5\left(g\right)\\ C\%_{Ba\left(OH\right)_2}=\dfrac{0,1.171}{265,5}.100=\dfrac{380}{59\%}= 6,44\%\\b)n_{Ba\left(OH\right)_2}=\dfrac{212,4.\dfrac{380}{59}\%}{171} =0,08\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{14,7.40\%}{98}=0,06\left(mol\right)\\ Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4+2H_2O\\ Lậptỉlệ:\dfrac{0,08}{1}>\dfrac{0,06}{2}\Rightarrow Ba\left(OH\right)_2dư\\ n_{BaSO_4}=n_{H_2SO_4}=0,06\left(mol\right)\\ m_{ddsaupu}=212,4+14,7-0,06.233=213,12\left(g\right)\\ n_{Ba\left(OH\right)_2pư}=n_{H_2SO_4}=0,06\left(mol\right)\\ n_{Ba\left(OH\right)_2dư}=0,08-0,06=0,02\left(mol\right)\\ \Rightarrow C\%_{Ba\left(OH\right)_2dư}=\dfrac{0,02.171}{213,12}.100=1,61\%\)
5. \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ n_{H_2}=n_{Fe}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ \Rightarrow\%m_{Fe}=\dfrac{0,1.56}{37,6}.100=14,89\%;\%m_{Fe_2O_3}=100-14,89=85,11\%\)


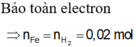
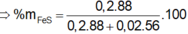
CTHH của X : $R_2O$
Ta có : $\%R = \dfrac{2R}{2R + 16}.100\% = 74,194\% \Rightarrow R = 23(Natri)$
$Na_2O + H_2O \to 2NaOH$
$m_{dd\ Y} = 15,5 + 184,5 = 200(gam)$
$n_{NaOH} = 2n_{Na_2O} = 2.\dfrac{15,5}{62} = 0,5(mol)$
$C\%_{NaOH} = \dfrac{0,5.40}{200}.100\% = 10\%$
Chọn đáp án B