Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đề bài tóm tắt:
- Nguyên tử Fe có:
- Bán kính nguyên tử: \(r = 1 , 28 \textrm{ } \overset{\circ}{\text{A}} = 1 , 28 \times 10^{- 10} \textrm{ } \text{m}\)
- Khối lượng mol nguyên tử: \(M = 56 \textrm{ } \text{g}/\text{mol} = 0 , 056 \textrm{ } \text{kg}/\text{mol}\)
- Trong tinh thể: nguyên tử chiếm 74% thể tích.
- Tính khối lượng riêng của Fe trong tinh thể.
Bước 1: Khối lượng của 1 nguyên tử Fe
Số Avogadro: \(N_{A} = 6 , 022 \times 10^{23}\) nguyên tử/mol
\(m_{\text{Fe}} = \frac{M}{N_{A}} = \frac{0 , 056}{6 , 022 \times 10^{23}}\) \(m_{\text{Fe}} \approx 9 , 30 \times 10^{- 26} \textrm{ } \text{kg}\)
Bước 2: Thể tích hình cầu nguyên tử Fe
\(V_{\text{c} \overset{ˋ}{\hat{\text{a}}} \text{u}} = \frac{4}{3} \pi r^{3} = \frac{4}{3} \pi \left(\right. 1 , 28 \times 10^{- 10} \left.\right)^{3}\) \(V_{\text{c} \overset{ˋ}{\hat{\text{a}}} \text{u}} \approx 8 , 78 \times 10^{- 30} \textrm{ } \text{m}^{3}\)
Bước 3: Thể tích thực tế trong mạng tinh thể
Do các nguyên tử chỉ chiếm 74% thể tích:
\(V_{\text{th}ự\text{c}\&\text{nbsp};\text{t} \overset{ˊ}{\hat{\text{e}}}} = \frac{V_{\text{c} \overset{ˋ}{\hat{\text{a}}} \text{u}}}{0 , 74}\) \(V_{\text{th}ự\text{c}\&\text{nbsp};\text{t} \overset{ˊ}{\hat{\text{e}}}} \approx \frac{8 , 78 \times 10^{- 30}}{0 , 74} \approx 1 , 19 \times 10^{- 29} \textrm{ } \text{m}^{3}\)
Bước 4: Khối lượng riêng
\(\rho = \frac{m_{\text{Fe}}}{V_{\text{th}ự\text{c}\&\text{nbsp};\text{t} \overset{ˊ}{\hat{\text{e}}}}} = \frac{9 , 30 \times 10^{- 26}}{1 , 19 \times 10^{- 29}}\) \(\rho \approx 7 , 8 \times 10^{3} \textrm{ } \text{kg}/\text{m}^{3}\)
✅ Kết quả:
\(\boxed{\rho \approx 7 , 8 \textrm{ } \text{g}/\text{cm}^{3} = 7 , 8 \times 10^{3} \textrm{ } \text{kg}/\text{m}^{3}}\)
cho tui 1 tick nha

Khối lượng riêng của Cr là 7,2 g/cm3;
nghĩa là 7,2 gam Cr ↔ 7,2 ÷ 52 × 6,023 × 1023 hạt nguyên tử Cr chiếm thể tích là 1cm3 = 10-6 m3.
Lại để ý: mỗi nguyên tử chỉ chiếm 68% thể tích tinh thể (còn lại là rỗng),
nghĩa là thể tích thực của mỗi nguyên tử Crom là:
V1 nguyên tử = 10-6 × 0,68 ÷ (7,2 ÷ 52 × 6,023 × 1023)) = 4 ÷ 3πr3.
Bấm fx CASIO có ngay r = 1,25 × 10-10 m = 0,125 nm.
ta chọn đáp án B.

Chọn A
Thể tích của 1 mol Fe là: 55 , 847 : 7 , 87 = 7 , 096 c m 3
Thể tích của một nguyên tử Fe là:
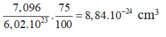
Bán kính gần đúng của nguyên tử Fe là:
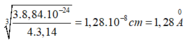

Đáp án C
Giả sử trong 1 mol Fe.
Thể tích thực của Fe là:

Thể tích 1 nguyên tử Fe là:
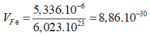
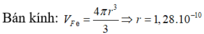

Đáp án A
xét 1 mol nguyên tủ Crom: có số nguyên tử Crom là 6.022. 10 23 nguyên tử và khối lượng là 52.
Thể tích của 1 mol nguyên tử Crom là:
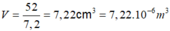
Thể tích thực của 1 nguyên tử Crom là:
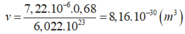
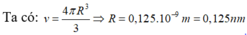

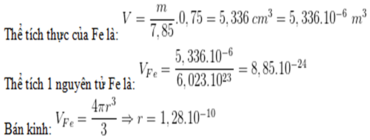
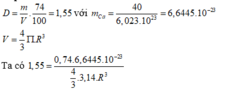
Đáp án A (tương tự câu 29)