Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{MnO_2} = \dfrac{4,35}{87} = 0,05(mol)\)
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
0,05..................................0,05..................(mol)
\(n_{NaOH} = 0,3.0,1 = 0,03(mol)\)
2NaOH + Cl2 → NaCl + NaClO + H2O
0,03........0,05.....0,015.......0,015....................(mol)
Vậy :
\(C_{M_{NaCl}} = C_{M_{NaClO}} = \dfrac{0,015}{0,3} = 0,05M\)

1/ Gọi x, y lần lượt là số mol của Na2CO3 và KHCO3.
Khi cho từ từ HCl vào dung dịch A thì các phản ứng xảy ra lần lượt là :
CO3^2- + H^+ => HCO3-
x ---------> x ----------> x
HCO3^- + H+ => H2O + CO2.
0,045 <--- 0,045 <-------- 0,045
.........HCO3^- + OH- => CO3^2- + H2O.
x+y - 0,045 -------------> x+y-0,045.
Giải hệ: x+y-0,045 = 29,55/197; n HCl = x+ 0,045 = 0,15.
=> x = 0,105 ; y = 0,09.
2/ Nồng độ của HCO3- , CO3^2- lần lượt là 0,225 M; 0,2625 M.
3/ Cho từ từ dung dịch A vào bình đựng 100 ml dung dịch HCl 1,5 M => Các phản ứng xảy ra đồng thời:
CO3^2- + 2 H^+ => H2O + CO2.
HCO3- + H+ => H2O + CO2.
Do tỉ lệ trong hỗn hợp : n CO3^2-/ n HCO3- = 7/6 => 7x*2+6x = 0,15 => x=0,0075.
=> V = 2,184 lít.

Bài tập vận dụng
VD1: Hoà tan hoàn toàn 7,45 gam KCI vào 200ml H2O thu đưoc dung dịch A. Tính nồng độ %, nồng độ mol/l
của dung dịch A.
VD2: Hoà tan hoàn toàn 0,2 mol NaOH vào 500ml H20 thu được dung dịch B. Tính nồng độ %, nồng độ mol/l
của dung dịch B.
VD3: Hoà tan hoàn toàn 2,8 gam KOH và 5,85 gam NaCl vào 600 ml H2O thu được dung dịch C. Tinh nồng độ
%, nồng độ mol/l của dung dịch C.
VD4: Hoà tan hoàn toàn 4,6 gam Na vào 100 gam H20 thu được dung dịch D. Tính nồng độ %, nồng độ mol/I
của dung dịch D.
VD5: Hoà tan hoàn toàn 2,74 gam Ba vào 200 gam H2O thu được dung dịch E. Tính nồng độ %, nồng độ mol/l
của dung dịch E.
VD6: Hoà tan hoàn toàn 5,85 gam K và 13,7 gam Ba vào 400ml H2O thu đưoc dung dịch F. Tính nồng đo %,
nồng đo mol/l của dung dịch F.
VD1:
\(n_{KCl}=\dfrac{7,45}{74,5}=0,1\left(mol\right)\\ V_{ddKCl}=V_{H_2O}=200\left(ml\right)=0,2\left(l\right)\\ C_{MddKCl}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)

Câu 1 :
\(n_{H_2SO_4}=0.2\cdot0.1=0.02\left(mol\right)\)
\(n_{KOH}=0.3\cdot0.1=0.03\left(mol\right)\)
\(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
\(2..............1\)
\(0.03............0.02\)
Lập tỉ lệ : \(\dfrac{0.03}{2}< \dfrac{0.02}{1}\) \(\Rightarrow H_2SO_4dư\)
\(n_{K_2SO_4}=\dfrac{0.03}{2}=0.015\left(mol\right)\)
\(n_{H_2SO_{4\left(dư\right)}}=0.02-0.015=0.005\left(mol\right)\)
\(V_{ddX}=0.2+0.3=0.5\left(l\right)\)
\(C_{M_{K_2SO_4}}=\dfrac{0.015}{0.5}=0.03\left(M\right)\)
\(C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0.005}{0.5}=0.01\left(M\right)\)
Câu 2 :
\(n_{H_2}=\dfrac{0.672}{22.4}=0.03\left(mol\right)\)
Hai kim loại ở 2 chu kỳ liên kết thuộc nhóm IA => Đặt CT chung là : M
\(M+H_2O\rightarrow MOH+\dfrac{1}{2}H_2\)
\(0.06............................0.03\)
\(M_M=\dfrac{0.6}{0.06}=10\)\(\Rightarrow9< 10< 23\)
Hai kim loại là : Li và Na
\(n_{Li}=a\left(mol\right),n_{Na}=b\left(mol\right)\)
\(m_{hh}=9a+23b=0.6\left(g\right)\left(1\right)\)
\(n_{H_2}=0.5a+0.5b=0.03\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.056,b=0.004\)
\(\%m_{Li}=\dfrac{0.056\cdot9}{0.6}\cdot100\%=84\%\)
\(\%m_{Na}=100-84=16\%\)

a,\(n_{H_2SO_4}=0,5.0,2=0,1\left(mol\right)\)
PTHH: H2SO4 + 2KOH → K2SO4 + 2H2O
Mol: 0,1 0,2 0,1
b,\(C_{M_{ddKOH}}=\dfrac{0,2}{0,05}=4M\)
c,Vdd sau pứ = 0,2+0,05 = 0,25 (l)
\(C_{M_{ddK_2SO_4}}=\dfrac{0,1}{0,25}=0,4M\)

Chọn D
Gọi N 2 C O 3 (x mol) và N a H C O 3 ( y mol)
Nhỏ từ từ HCl vào hỗn hợp xảy ra pư theo thứ tự:
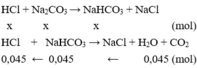

a, Ta có :
0,2l dung dịch HCl thì có nồng độ 0,1M
Suy ra 0,016l dd HCl thì có nồng độ xM
\(\rightarrow x=\frac{0,016.0,1}{0,2}=0,008\left(\frac{mol}{l}\right)\)
b, \(CM_{HCl}=\frac{0,01.0,1}{0,2}=0,005\left(mol\right)\)
\(\rightarrow n_{HCl}=0,005.0,01=0,0005\left(mol\right)\)
\(\rightarrow n_{KOH}=0,015.0,85=0,01275\left(mol\right)\)
\(PTHH:KOH+HCl\rightarrow KCl+H_2O\)
Theo phương trình : KOH dư , sau pứng tính theo HCl
\(m_{dd}=0,01+0,015=0,025\left(g\right)\)
\(CM_{KCl}=\frac{0,0005}{0,025}=0,002M\)
\(CM_{KOH}=\frac{0,01275-0,0005}{0,025}=0,508M\)