Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Al không tác dụng với $HNO_3$ đặc nguội
$Cu + 4HNO_3 \to Cu(NO_3)_2 + 2NO_2 + 2H_2O$
$n_{Cu} = \dfrac{1}{2}n_{NO_2} = \dfrac{1}{2}.\dfrac{3,36}{22,4} = 0,075(mol)$
Mặt khác : $n_{NO} = \dfrac{7,84}{22,4} = 0,35(mol)$
Bảo toàn electron : $2n_{Cu} + 3n_{Al} = 3n_{NO}$
$\Rightarrow n_{Al} = \dfrac{0,35.3 - 0,075.2}{3} = 0,3(mol)$
$m = 0,075.64 + 0,3.27 = 12,9(gam)$

\(Đặt:\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{matrix}\right.\\ Fe\rightarrow Fe^{3+}+3e\\ Cu\rightarrow Cu^{2+}+2e\\ 4H^++NO_3^-+3e\rightarrow NO+2H_2O\\ Bảotoàne:3x+2y=0,4.3\\ Tacó:56x+64y=30,4\\ \Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=36,84\%\\\%m_{Cu}=63,16\%\end{matrix}\right.\\ n_{HNO_3}=4n_{NO}=0,4.4=1,6\left(mol\right)\\ \Rightarrow V_{HNO_3}=\dfrac{1,6}{1}=1,6\left(l\right)\\ m_{muối}=m_{Fe\left(NO_3\right)_3}+m_{Cu\left(NO_3\right)_2}=0,2.242+0,3.188=104,8\left(g\right)\)

Chọn D
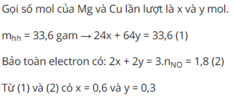
Khối lượng Mg, Cu trong hỗn hợp lần lượt là 14,4 gam và 19,2 gam.

nHNO3 ban đầu = 1,425
MX = 32,8; Sử dụng sơ đồ đường chéo ⇒ n NO = 0,2 ; n N2O = 0,05
Ta có nNO3- trong muối kl = ne = 8nN2O + 8nNH4NO3
Bảo toàn nguyên tố N: nHNO3 ban đầu = n NO + 2n N2O + 2n NH4NO3 + n NO3- trong muối KL
⇒ nHNO3 ban đầu = 4 nNO + 10 nN2O + 10 nNH4NO3
⇒ nNH4NO3 = 0,0125
⇒ nNO3-/muối KL= 1,1
⇒ m = mNO3-/muối kl + mKL + mNH4NO3 = 1,1.62 +29 + 0,0125.80 = 98,2g
Đáp án A.

nHNO3 ban đầu = 1,425
MX = 32,8; Sử dụng sơ đồ đường chéo ⇒ n NO = 0,2 ; n N2O = 0,05
Ta có nNO3- trong muối kl = ne = 8nN2O + 8nNH4NO3
Bảo toàn nguyên tố N: nHNO3 ban đầu = n NO + 2n N2O + 2n NH4NO3 + n NO3- trong muối KL
⇒ nHNO3 ban đầu = 4 nNO + 10 nN2O + 10 nNH4NO3
⇒ nNH4NO3 = 0,0125
⇒ nNO3-/muối KL= 1,1
⇒ m = mNO3-/muối kl + mKL + mNH4NO3 = 1,1.62 +29 + 0,0125.80 = 98,2g
Đáp án A.

Đáp án A
nNO = 2,8/22,4 = 0,125 (mol)
BTNT N: nNO3 ( trong muối) = 3nNO = 0,375 (mol)
=> mmuối = mKL + mNO3- = 7,55 + 0,375.62 = 30,8 (g)
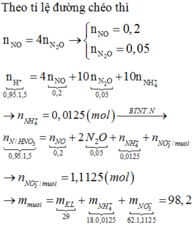
\(Al\rightarrow Al^{3+}+3e\\ Cu\rightarrow Cu^{2+}+2e\\ N^{+5}+3e\rightarrow N^{+2}\\ Đặt:\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{matrix}\right.\\ n_{NO}=\dfrac{31,36}{22,4}=1,4\left(mol\right)\\ BTe:3x+2y=1,4.3\\ Mặtkhác:27x+64y=65,4\\ \Rightarrow\left\{{}\begin{matrix}x=1\\y=0,6\end{matrix}\right.\\ \Rightarrow\%m_{Cu}=\dfrac{0,6.64}{65,4}.100=58,72\%\\ \Rightarrow ChọnC\)