Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
Ta có: \(n_{C_2H_4}+n_{C_2H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\left(1\right)\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}+n_{C_2H_2}=\dfrac{6,4}{160}=0,04\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_4}=0,01\left(mol\right)\\n_{C_2H_2}=0,015\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,01.22,4}{0,56}.100\%=40\%\\\%V_{C_2H_2}=60\%\end{matrix}\right.\)

- Phần 1 tác dụng với Br2: nBr2 = 16:160 = 0,1 mol
C2H2 + 2Br2 → C2H2Br4
0,05 ← 0,1 (mol)
- Đặt số mol khí mỗi phần như sau:
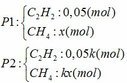
+ Số mol hỗn hợp khí X là: nX = 11,2:22,4 = 0,5 mol
Ta có: n khí P1 + n khí P2 = nX => 0,05 + x + 0,05k + kx = 0,5 <=> (x + 0,05)k = 0,45 - x
=> 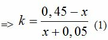
+ Đốt cháy phần 2:
C2H2 + 2,5O2 → t ∘ 2CO2 + H2O
0,05k → 0,1k→ 0,05k (mol)
CH4 + 2O2 → t ∘ CO2 + 2H2O
kx → kx → 2kx (mol)
Sản phẩm cháy gồm
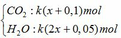
dẫn qua dung dịch Ba(OH)2 dư:
CO2 + Ba(OH)2 → BaCO3↓ + H2O
k(x+0,1) → k(x+0,1) (mol)
Khối lượng dung dịch giảm: m dd giảm = mBaCO3 – mCO2 – mH2O
=> 197k(x+0,1) – 44k(x+0,1) – 18k(2x+0,05) = 69,525
=> 153k(x+0,1) – 18k(2x+0,05) = 69,525
=> k(117x+14,4) = 69,525
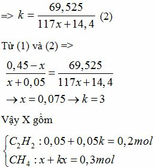
CaC2 + 2H2O → Ca(OH)2 + C2H2
0,2 ← 0,2 (mol)
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
0,1 ← 0,1 (mol)
Giá trị của m là: m = mCaC2 + mAl4C3 = 0,2.64 + 0,1.144 = 27,2 gam
Phần trăm thể tích các khí trong X là:

tác dụng với AgNO3 trong NH3 dư:
C2H2 + 2AgNO3 + 2NH3 → Ag2C2↓ + 2NH4NO3
0,15 → 0,15 (mol)
Khối lượng kết tủa thu được là: mAg2C2 = 0,15.240 = 36 gam

C2H4+Br2->C2H4Br2
x----------x---------x
C2H2+2Br2->C2H2Br4
y--------2y------------y
=>\(\left\{{}\begin{matrix}x+y=\dfrac{0,896}{22,4}\\160x+320y=8\end{matrix}\right.\)
=>x=0,03 mol, y=0,01 mol
=>%VC2H4=\(\dfrac{0,03.22,4}{0,896}\).100=75%
=>%VC2H2=25%

\(n_{hh}=\dfrac{2,8}{22,4}=0,125mol\)
\(n_{Br_2}=\dfrac{4}{160}=0,025mol\)
\(n_{Br_2}=n_{C_2H_4}=0,025mol\)
\(\%V_{C_2H_4}=\dfrac{0,025}{0,125}.100=20\%\)
\(V_{CH_4}=100\%-20\%=80\%\)
=> Chọn D

\(n_{hh.khí}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\\ n_{Br_2}=\dfrac{4}{160}=0,025\left(mol\right)\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Khí metan không tác dụng với dd Br2
\(n_{C_2H_4}=n_{Br_2}=0,025\left(mol\right)\)
Vì số mol tỉ lệ thuận với thể tích. Nên:
\(\%V_{C_2H_4}=\%n_{C_2H_4}=\dfrac{0,025}{0,125}.100=20\%\\ \Rightarrow\%V_{CH_4}=100\%-20\%=80\%\)
Vậy chọn D
Chúc em học tốt và có được POP!
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(n_{Br_2}=\dfrac{4}{160}=0,025mol\)
\(V_{Br_2}=0,025.22,4=0,56l\)
\(\%V_{C_2H_4}=\dfrac{0,56.100}{2,8}=20\%\)
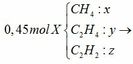



\(n_A=\dfrac{4,48}{22,4}=0,2mol\\ n_{Br_2}=\dfrac{48}{160}=0,3mol\\ n_{C_2H_4}=a;n_{C_2H_2}=b\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ C_2H_2+2Br_2\rightarrow C_2H_2Br_4\\ \Rightarrow\left\{{}\begin{matrix}a+b=0,2\\a+2b=0,3\end{matrix}\right.\\ \Rightarrow a=b=0,1\\ \Rightarrow A\)