Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a.\left\{{}\begin{matrix}CO_2\\Ca\left(OH\right)_2\end{matrix}\right.\rightarrow CaCO_3\rightarrow Ca\left(HCO_3\right)_2\)
\(b.\) \(n_{CaCO_3}=0,05\left(mol\right)\)
\(PTHH:CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
\(\left(mol\right)\) \(0,05\) \(0,05\) \(0,05\)
\(PTHH:CaCO_3+CO_2+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
\(\left(mol\right)\) \(0,05\) \(0,05\) \(0,05\)
\(\rightarrow V_{CO_2}=22,4.\left(0,05+0,05\right)=2,24\left(l\right)\)
\(c.V_{Ca\left(OH\right)_2}=\dfrac{0,05}{0,1}=0,5\left(l\right)\\ m_{Ca\left(HCO_3\right)_2}=0,05.162=8,1\left(g\right)\\ C_{M_{Ca\left(HCO_3\right)_2}}=\dfrac{0,05}{0,5}=0,1\left(M\right)\)
\(d.V_{CO_2}=0,05.22,4=1,12\left(l\right)\\ m_{\downarrow}=5\left(g\right)\)
a) Dẫn từ từ CO2 đến dư vào dung dịch Ca(OH)2 xảy ra phản ứng:
CO2 + Ca(OH)2 → CaCO3 + H2O
CO2 + CaCO3 + H2O → Ca(HCO3)2
Hiện tượng quan sát được: Dung dịch xuất hiện kết tủa trắng tăng dần đến cực đại, sau đó kết tủa tan dần đến hết.
b)\(n_{CaCO_3}=\dfrac{5}{100}=0,05\left(mol\right)\)
CO2 + Ca(OH)2 → CaCO3 + H2O
0,05<---0,05------------0,05
CO2 + CaCO3 + H2O → Ca(HCO3)2
0,05<----0,05-------------------->0,05
Theo PT ta có : \(n_{CO_2}=2n_{CaCO_3}=0,1\left(mol\right)\)
=> \(V_{CO_2}=0,1.22,4=2,24\left(l\right)\)
c)Theo PT ta có : \(n_{Ca\left(HCO_3\right)_2}=n_{CaCO_3}=0,05\left(mol\right)\)
=> \(m_{Ca\left(HCO_3\right)_2}=0,05.162=8,1\left(g\right)\)
Theo PT ta có : \(n_{Ca\left(OH\right)_2}=n_{CaCO_3}=0,05\left(mol\right)\)
\(V_{Ca\left(OH\right)_2}=\dfrac{0,05}{0,1}=0,5\left(l\right)\)
Giả sử thể tích dung dịch thay đổi không đáng kể:
=> \(CM_{Ca\left(HCO_3\right)_2}=\dfrac{0,05}{0,5}=0,1M\)
d) Trường hợp chỉ tạo ra kết tủa :
CO2 + Ca(OH)2 → CaCO3 + H2O
Theo PT : \(n_{CO_2}=n_{CaCO_3}=n_{Ca\left(OH\right)_2}=0,05\left(mol\right)\)
=> \(V_{CO_2}=0,05.22,4=1,12\left(l\right)\)
\(m_{CaCO_3}=0,05.100=5\left(g\right)\)

được.Vì:
2SO2 + Ca(OH)2 dư \(\rightarrow\) Ca(HSO3)2
H2S + Ca(OH)2 \(\rightarrow\) CaS \(\downarrow\) + 2H2O

Những chất nào sau đây có thể được dùng để làm khô khí lưu huỳnh đioxit bị ẩm?
A. CaO
B. H2SO4 đặc
C. Ca(OH)2
D. CuSO4 khan
Nguyên tắc làm khô khí là khí đó phải KHÔNG phản ứng với chất làm khô
=> Chọn B, D

Câu 6. Để làm sạch mẫu kim loại đồng có lẫn kim loại sắt và kẽm, có thể ngâm mẫu đồng này vào dung dịch:
a. FeCl2 dư b. ZnCl2 dư c. CuCl2 dư d. AlCl3 dư
Câu 7.Dung dịch ZnCl2 bị lẫn tạp chất là CuCl2. Có thể làm sạch dung dịch ZnCl2 này bằng kim loại:
a. Zn b. Mg c. Na d. Cu
Câu 8: Nhận biết 3 kim loại: Al, Ag, Fe bằng các thuốc thử:
A. Dung dịch HCl và dung dịch AgNO3
B. Dung dịch CuSO4 và dung dịch BaCl2
C. Dung dịch NaOH và dung dịch HCl
D. Dung dịch HCl và dung dịch NaCl
Câu 9.Dữ kiện nào dưới đây cho thấy nhôm hoạt động hóa học mạnh hơn sắt:
A. Al, Fe đều không phản ứng với HNO3 đặc nguội và H2SO4 đặc nguội.
B. Al có phản ứng với dung dịch kiềm
C. Nhôm đẩy được sắt ra khỏi dung dịch muối sắt
D. Chỉ có sắt bị nam châm hút
Câu 10.Cây đinh sắt trong trường hợp nào dưới đây bị gỉ sét nhanh và nhiều hơn:
A.Để ngoài không khí ẩm. B. Ngâm trong dầu ăn.
C.Ngâm trong dung dịch nước muối D. Ngâm trong nhớt máy.
Câu 11.Không được dùng chậu nhôm để chứa nước vôi trong vì:
A.Nhôm tác dụng được với dung dịch axit.
B.Nhôm tác dụng được với dung dịch bazo.
C.Nhôm đẩy được kim loại yếu hơn nó ra khỏi dung dịch muối.
D.Một lý do khác.
Câu 12.Kim loại nào dưới đây vừa tác dụng với dung dịch HCl, vừa tác dụng với dung dịch NaOH:
A.Fe B. Cu C. Al D. Ag
Câu 13.Có một mẫu sắt bị lẫn tạp chất là nhôm. Có thể làm sạch mẫu sắt này bằng cách ngâm nó vào:
A.Dung dịch NaOH dư B. Dung dịch H2SO4 dư
C.Dung dịch HCl dư D. Nước cất
Câu 14.Có 3 lọ đựng 3 chất riêng biệt: Mg, Al, Al2O3. Chỉ dùng một thuốc thử để nhận biết được cả 3 chất rắn trên. Thuốc thử cần dùng là dung dịch chất nào sau đây?
A. HCl B. H2O C. HNO3 D. NaOH
Câu 15: Ngâm một đinh sắt sạch trong dung dịch CuSO4 loãng, hiện tượng xảy ra là:
A. Sủi bọt khí, màu xanh của dung dịch nhạt dần
B. Kim loại đồng màu đỏ bám ngoài đinh sắt, màu xanh của dung dịch đậm dần
C. Kim loại đồng màu đỏ bám ngoài đinh sắt, dung dịch không đổi màu
D. Một phần đinh sắt bị hòa tan, màu xanh của dung dịch nhạt dần, kim loại đồng màu đỏ bám ngoài đinh sắt
Câu 16: Bình làm bằng nhôm có thể dùng để đựng axit nào sau đây?
A. H3PO4 đặc nguội C. HCl
B. HNO3 đặc nguội D. HNO3 đặc nóng

Có 2 phương trình bạn nhé!!!
4Ag + 2H2S + O2 → 2H2O + 2Ag2S
2Ag + H2S → H2 + Ag2S
4Ag + 2H2S + O2 \(\rightarrow\) 2H2O + 2Ag2S\(\downarrow\)
hoặc:
2Ag + H2S (ẩm) \(\rightarrow\) H2 + Ag2S \(\downarrow\)
Ag2S kết tủa đen

Các hiện tượng đó được giải thích dựa trên cơ sở là dầu mỡ ăn ít tan trong nước lạnh, tan nhiều hơn trong nước nóng.

Bình thường trông bên ngoài nước không có vấn đề gì, thực tế trong nước có hòa tan nhiều chất, thường gặp nhất là các muối canxi, magiê và sắt. Các nguồn nước có thể chứa lượng muối sắt ít nhiều khác nhau, loại nước chứa nhiều sắt “ là thủ phạm” làm cho nồi nhôm có màu đen.
Vì nhôm có tính khử mạnh hơn sắt nên nhôm sẽ đẩy sắt ra khỏi muối của nó và thay thế ion sắt, còn ion sắt bị khử sẽ bám vào bề mặt nhôm, nồi nhôm sẽ bị đen: Để hoàn thành được điều trên phải có 3 điều kiện: Lượng muối sắt trong nước phải đủ lớn; Thời gian đun sôi phải đủ lâu; Nồi nhôm phải là nồi mới
p/s: tham khảo nha
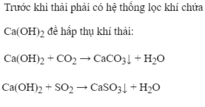
giúp mình vs:((((((((
Tham khảo:
Cảm là trạng thái con người nhiễm các khí độc qua "da". Gió độc thấm vào cơ thể qua da tại các "lỗ chân lông". Các khí đó hầu hết là hợp chất của lưu huỳnh. Khi đánh bằng Ag có 2 tác dụng:
- Ag tác dụng với các khí của S tạo thành hợp chất Ag2S có màu đen. Ag và Hg là 2 kim loại phản ứng dễ dàng với S (do tạo thành hợp chất rất rất khó tan - đặc biệt là Hg). Khi lượng khí độc được loại bỏ (bằng cách dùng Ag) thì cơ thể phục hồi trở lại.
- Ag có tác dụng diệt khuẩn. Chẳng thế mà từ thời thượng cổ người ta đã biết dùng các đồ bằng Ag như bát, đũa ... để đựng thức ăn.