Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTPƯ:
FexOy + 2yHCI -------------> xFeCI2y/x +yH2O
1mol ----------------------------> xmol
16/(56x +16y)mol-------------> 32,5/(56 + 71y/x)
=> 16x/(56x + 16y) = 32,5/(56 + 71y/x)
=> 896x +1136y = 1820x + 520y
=>616y = 924x
=> x/y = 2/3
Vậy CT của oxít sắt là Fe2O3

Vì sau phản ứng chỉ thu được 1 oxit sắt nên oxit sắt không phải là oxi sắt từ.
Gọi CT oxit là Fe2Oa
Fe2Oa(\(\dfrac{10,8}{112+16a}\))+2aHCl→2FeCla(\(\dfrac{10,8}{56+8a}\))+aH2O
nFe2Oa=\(\dfrac{10,8}{112+16a}\)
⇒\(\dfrac{10,8}{56+8a}.\left(56+35,5a\right)=19,05\)
⇔a=2
Vậy CT của oxit sắt là FeO

CTHH của oxit sắt là FexOy
nfe =22,4/56=0,4 mol
pt : FexOy + yCO-> x Fe + y CO2
npứ : 0,4
Ta có : mFexOy =32g và mFexOy= mfe + mO
<=> mo= mFexOy - mfe
<=>mo=32-(0,4.56)=9,6g
=>no=9,6/16=0,6mol
=> x/y = nfe/no =0 ,4/0,6 =2/3
CTHH :Fe2 O3
Gọi CTHH của oxit sắt là FexOy
FexOy + yCO → xFe + yCO2
\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
theo pT: \(n_{Fe_xO_y}=\dfrac{1}{x}n_{Fe}=\dfrac{1}{x}\times0,4=\dfrac{0,4}{x}\left(mol\right)\)
Ta có: \(M_{Fe_xO_y}=32\div\dfrac{0,4}{x}\)
\(\Leftrightarrow160=80x\)
\(\Leftrightarrow x=2\)
Ta có: \(56\times2+16y=160\)
\(\Leftrightarrow112+16y=160\)
\(\Leftrightarrow16y=48\)
\(\Leftrightarrow y=3\)
Vậy CTHH của oxit sắt là Fe2O3

1 ) CAO +H2O => CA(OH)2 (1)
2K + 2H2O => 2KOH + H2(2)
n (H2) =1,12/22,4 =0,05
theo ptpư 2 : n(K) = 2n (h2) =2.0.05=0,1(mol)
=> m (K) =39.0,1=3,9 (g)
% K= 3,9/9,5 .100% =41,05%
%ca =100%-41,05%=58,95%
xo + 2hcl =>xcl2 +h2o
10,4/X+16 15,9/x+71
=> giải ra tìm đc X bằng bao nhiêu thì ra

Gọi số mol CO=mol CO2= a mol
Bảo toàn klg=>23,2+28a=44a+16,8
=>a=0,4 mol
=>VCO2=0,4.22,4=8,96 lit
Gọi CT oxit là Fe2On
Bảo toàn Fe: nFe tạo thành=nFe trong oxit ban đầu=16,8/56=0,3 mol
=>n oxit sắt=0,15 mol
=>M oxit sắt=23,2/0,15=464/3 =>n=8/3 CT oxit sắt là Fe3O4
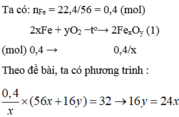
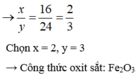

Tham khảo:
a) Ta có: nFe = 22,4/56 = 0,4 (mol)
2xFe + yO2 −to→ 2FexOy (1)
(mol) 0,4 → 0,4/x
Theo đề bài, ta có phương trình :
0,4/x(56x + 16y) = 32 → 16y = 24x → x/y= 16/24= 2/3
Chọn x=2, y=3 → Công thức oxit sắt : Fe2O3.
b) Hoá trị của sắt trong Fe2O3 là : III.
Tham khảo
a) Ta có: nFe = 22,4/56 = 0,4 (mol)
2xFe + yO2 −to→ 2FexOy (1)
(mol) 0,4 → 0,4/x
Theo đề bài, ta có phương trình :
0,4/x(56x + 16y) = 32 → 16y = 24x → x/y= 16/24= 2/3
Chọn x=2, y=3 → Công thức oxit sắt : Fe2O3.
b) Hoá trị của sắt trong Fe2O3 là : III.