Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Br_2}=\dfrac{5,6}{160}=0,035\left(mol\right)\)
PTHH: C2H2 + 2Br2 --> C2H2Br4
0,0175<-0,035
=> \(\%V_{C_2H_2}=\dfrac{0,0175.22,4}{0,56}.100\%=70\%\)
=> %VCH4 = 100% - 70% = 30%
=> B

Số mol hỗn hợp = 0m56 : 22,4 = 0,025 mol; số mol Br2 = 5,6 : 160 = 0,035 mol.
Gọi x, y lần lượt là số mol của etilen và axetilen.
a) Phương trình hoá học:
C2H4 + Br2 → C2H4Br2
P.ư: x x x (mol)
C2H2 + 2Br2 → C2H2Br4
P.ư: y 2y y (mol)
b) Ta có hệ phương trình: ; Giải hệ ta được y = 0,01 và x = 0,015
% =
x 100% = 60%;
= 100% - 60% = 40%

a, PT: \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
b, \(n_{Br_2}=\dfrac{5,6}{160}=0,035\left(mol\right)\)
Theo PT: \(n_{C_2H_2}=\dfrac{1}{2}n_{Br_2}=0,0175\left(mol\right)\)
\(\Rightarrow\%V_{C_2H_2}=\dfrac{0,0175.22,4}{0,86}.100\%\approx45,58\%\)
\(\Rightarrow\%V_{CH_4}\approx54,42\%\)

a, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
Giả sử: \(\left\{{}\begin{matrix}n_{C_2H_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{1,344}{22,4}=0,06\left(1\right)\)
Ta có: \(n_{Br_2}=\dfrac{16}{160}=0,1\left(mol\right)\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}+2n_{C_2H_2}=x+2y\left(mol\right)\)
⇒ x + 2y = 0,1 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,02\left(mol\right)\\y=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,02}{0,06}.100\%\approx33,33\%\\\%\text{ }V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Ta có: 1/2 hỗn hợp khí gồm: 0,01 mol C2H4 và 0,02 mol C2H2.
PT: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Theo PT: \(n_{CO_2}=2n_{C_2H_4}+2n_{C_2H_2}=0,06\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=0,06\left(mol\right)\)
\(\Rightarrow m_{cr}=m_{CaCO_3}=0,06.100=6\left(g\right)\)
Bạn tham khảo nhé!

nBr2 = 0,125 mol
Khi đốt cháy nA = 0,25 mol
mNaOH ban đầu = 36g => nNaOH = 0,9 mol
Gọi x, y lần lượt là số mol của CO2 và H2O
mdd = 180 + 44x + 18y
Vì NaOH dư do đó chỉ tạo muối trung hòa
CO2 +2NaOH → Na2CO3 + H2O
x 2x
nNaOH dư = 0,9 – 2x
có 2 , 75 % = 40 ( 0 , 9 - 2 x ) 180 + 44 x + 18 y . 100 % (1)
=> 81,21x + 0,495y = 31,05n
2,8 lít khí A tác dụng với 0,125 mol Br2
=> 5,6 lít khí A tác dụng với 0,25 mol Br2
Gọi số mol khí của CH4, C2H4 và C2H2 lần lượt là a; b; c
Ta có a + b + c = 0,25 mol
Và b + 2c = 0,25
=> a = c
=> khi đốt cháy hỗn hợp A cho nCO2 = nH2O
Thay vào (1) => x = y = 0,38 mol
Bảo toàn C, H khi đốt cháy ta có
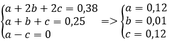
=> %VCH4 = %VC2H2 = 48%
%VC2H4 = 4%

a)
C2H4 + Br2 --> C2H4Br2
C2H2 + 2Br2 --> C2H2Br4
b) Gọi số mol C2H4, C2H2 là a, b (mol)
=> \(a+b=\dfrac{11,2}{22,4}=0,5\) (1)
PTHH: C2H4 + Br2 --> C2H4Br2
a---->a
C2H2 + 2Br2 --> C2H2Br4
b---->2b
=> a + 2b = \(\dfrac{112}{160}=0,7\) (2)
(1)(2) => a = 0,3 (mol); b = 0,2 (mol)
\(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,3}{0,5}.100\%=60\%\\\%V_{C_2H_2}=\dfrac{0,2}{0,5}.100\%=40\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{C_2H_4}=\dfrac{0,3.28}{0,3.28+0,2.26}.100\%=61,765\%\\\%m_{C_2H_2}=\dfrac{0,2.26}{0,3.28+0,2.26}.100\%=38,235\%\end{matrix}\right.\)

Mạnh dạn đoán đây là Bài 5 trang 122 sgk Hóa lớp 9.
Đề bài bạn gửi bị thiếu một khí nữa là C2H4 đúng không?
Bạn xem lại đề bài nhé, nếu đúng là hỗn hợp khí gồm C2H2 và C2H4 thì mình giải như sau:
Gọi số mol của C2H4 và C2H2 lần lượt là x và y mol theo bài ra: x+y = 0,56/22,4 = 0,025 (mol)
(1) Pt: C2H4 + Br2 → C2H4Br2
x mol x mol x mol
C2H2 + 2 Br2 → C2H2Br4
y mol 2y mol y mol
Số mol n Br2 = x+2y = 5,6/160 = 0,035 9mol) (2)
Giải hệ (1) và (2) ta đc: x = 0,015 và y = 0,01
=> %V C2H4 = 0,015/0,025 = 60% ;
%V C2H2 = 40% (%V = % số mol ở cùng điều kiện)

Câu 1: A
Câu 2: A
Câu 3: B
Câu 1: Dẫn 0,1 mol khí axetilen qua dung dịch nước brom dư. Khối lượng brom tham gia phản ứng là
A. 16,0 gam. B. 20,0 gam.
C. 26,0 gam. D. 32,0 gam.
Câu 2: Đốt cháy hoàn toàn 5,6 lít khí C2H2 trong bình chứa khí oxi dư. Thể tích khí CO2 thu được (trong cùng điều kiện nhiệt độ và áp suất) là
A. 11,2 lít. B. 16,8 lít.
C. 22,4 lít. D. 33,6 lít.
Câu 3: Cho 0,56 lít (đktc) hỗn hợp khí metan và axetilen tác dụng với dung dịch brom dư, lượng brom đã tham gia phản ứng là 5,6 gam. Thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu lần lượt là
A. 20%; 80%. B. 30%; 70%.
C .40% ; 60%. D. 60%; 40%.