Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nNO = \(\dfrac{6,72}{22,4}\) = 0,300 (mol)
nHNO3nHNO3 = 1,00 x 1,5 = 1,5 (mol)
pthh: 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O (1)
Theo (1) ta tính được nCu = 0,45 mol => mCu = 28,8 gam
nHNO3nHNO3 = 1,2 mol
nCu(NO3)2nCu(NO3)2 = 0,45 mol
mCuO = 30 gam – 28,8 gam = 1,2 gam => nCuO = 0,015 mol
CuO + 2HNO3 → Cu(NO3)2 + H2O (2)
Theo (2) ta tính được nHNO3nHNO3 là 0,030 mol, nCu(NO3)2nCu(NO3)2 là 0,015 mol
Phần tram khối lượng CuO: % mCuO = \(\dfrac{1,2}{30}\) . 100% = 4,0 %
Từ (1) và (2) ta tính được số mol HNO3 dư là 0,27 mol.
Nồng độ mol HNO3 sau phản ứng: 0,18 M
Nồng độ mol của Cu(NO3)2: 0,31 M

Phương trình hoá học ở dạng phân tử và dạng ion rút gọn của các phản ứng xảy ra trong dung dịch :
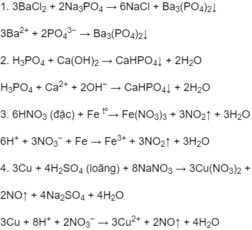

n HNO3 = 1,5 . 1 = 1,5 mol
n NO = 6,72 / 22,4 = 0,3 (mol)
0 +2
Cu -> Cu + 2e
0,45 <--------- 0.9
+5 +2
N + 3e -> NO
0.9 <- 0.3
m Cu = 0.45 . 64 =28.8 (g)
m CuO = 30 - 28,8 = 1,2 (g)
% m CuO = 1,2 / 30 x 100% = 4%
4H(+) + NO3(-) --> NO + 2H2O
1,2 <------ 0,3 <------ 0.3
n CuO = 1,2 / 80 = 0,015 (mol)
2HNO3 + CuO --> Cu(NO3)2 + H2O
0.03 <----- 0,015
=> n HNO3 còn = 1,5 - 1,2 - 0,03 = 0,27 (mol)
CM HNO3 = 0,27 / 1,5 = 1,8 M
CM Cu(NO3)2 = 0,465 / 1,5 = 0,31 M

nHNO3 = 1,5. 1,00 = 1,50 (mol)
nNO = 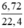 = 0,3(mol)
= 0,3(mol)
PTHH: 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O (1)
CuO + 2HNO3 → Cu(NO3)2 + H2O (2)
Theo pt(1) nCu = 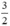 . nNO =
. nNO = 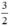 . 0,3 = 0,45 mol
. 0,3 = 0,45 mol
Gọi nCuO = x mol
Ta có: mhỗn hợp = mCu + mCuO = 0,45. 64 + 80x = 30,00
⇒ x = 0,015 ⇒ nCuO = 0,015 mol ⇒ mCuO = 0,015. 80 = 1,2 g
(Hoặc mCuO = 30 - 0,45. 64 = 1,2g)
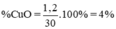
Theo pt(1) nCu(NO3)2 = nCu = 0,45 mol
Theo pt(2) nCu(NO3)2 = nCuO = 0,015 mol
⇒ Tổng nCu(NO3)2 = 0,45 + 0,015 = 0,465(mol)
CMCu(NO3)2 = 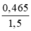 = 0,31(M)
= 0,31(M)
Theo pt (1) nHNO3 = 4. nNO = 4. 0,3 = 1,2 mol
Theo pt (2) nHNO3 = 2. nCuO= 2. 0,015 = 0,03 mol
nHNO3 (dư)= 1,5 - 1,2 – 0,03 = 0,27(mol)
CM HNO3 = 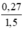 = 0,18(M)
= 0,18(M)

Phản ứng giữa dung dịch axit và hiđroxit có tính bazơ rất dễ xảy ra vì có sự tạo thành chất điện li rất yếu là H2O Ví dụ: Mg(OH)2 + 2HCl \(\rightarrow\) MgCl2 + 2H2O
Phản ứng giữa muối cacbonat và dung dịch axit dễ xảy ra vì có sự tạo thành chất khí là CO2
Ví dụ: Na2CO3 + 2HCl \(\rightarrow\) 2NaCl + CO2 \(\uparrow\)+ H2O

Chọn Đáp án đúng:
C. Có ba chất có khả năng làm mất màu dung dịch Brom

1.PTHH: Ba+MgCl2→BaCl2+Mg↓
Hiện tượng: Có Kết tủa màu trắng bạc
2. Ba+Mg(HCO3)2+2H2O→BaCO3↓+MgCO3↓+2H3O
Hiện tượng : Có kết tủa màu trắng..
3. Ba+FeCl2→BaCl2+Fe↓
Hiện tượng : Kết tủa màu trắng xám
Đáp án: A.