Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1)
1,2 tấn = 1200(kg)
5 tạ = 500(kg)
mCaCO3=1200.80%=960(kg)mCaCO3=1200.80%=960(kg)
CaCO3to→CaO+CO2nCaCO3 pư=nCaO=50056(mol)⇒H=50056.100960.100%=93%
\(m_{\text{CaCO_3}}=1000.95\%=950kg\\ \rightarrow n_{\text{CaCO_3}}=9,5mol\)
\(m_{CaCO_3}\underrightarrow{t^o}CaO+CO_2\)
9,5 → 9,5
\(\rightarrow V_{CO_2}=9,5.22,4=212,8\)
→ hiệu suất phản ứng là
\(\dfrac{159,6}{212,8}.100=75\%\)

Ta có phương trình hóa học :
\(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
Theo phương trình :
Cứ \(1\) mol \(CaCO_3\) nhiệt phân tạo 1 mol CaO
Hay 100g CaCO3 nhiệt phân tạo 56g CaO
Hay 100 tấn CaCO3 nhiệt phân tạo 56 tấn CaO
Vậy khối lượng CaCO3 tạo ra 1,4 tấn CaO là :
\(m_{CaCO3.pư}=\dfrac{1,4.100}{56}=2,5\)(tấn)
Do hiệu suất 80% nên khối lượng CaCO3 ban đầu là :
\(m_{CaCO3.bđ}=\dfrac{2,5}{80\%}=3,125\) ( tấn )
Khối lượng đá vôi đem đi nung là :
\(m=\dfrac{3,125}{75\%}=4,167\)( tấn )
CaCO3 -to->CaO + CO2
100 56
2,5 ← 1,4
mCaCO3 (lý thuyết) = \(\dfrac{2,5.100}{80}\)= 3,125 gam (tấn) (đề bài không rõ đơn vị)
Khối lượng đá vôi = \(\dfrac{3,125.100}{75}\)= 4,17 gam (tấn)

Phương trình hóa học CaCO3 → CaO + CO2.
a) nCaO = 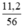 = 0,2 mol.
= 0,2 mol.
Theo PTHH thì nCaCO3 = nCaO = 0,2 (mol)
b) nCaO = 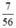 = 0,125 (mol)
= 0,125 (mol)
Theo PTHH thì nCaCO3 = nCaO = 0,125 (mol)
mCaCO3 = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO2 = nCaCO3 = 3,5 (mol)
VCO2 = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO2 = 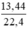 = 0,6 (mol)
= 0,6 (mol)
Theo PTHH nCaO = nCaCO3 = nCO2 = 0,6 (mol)
mCaCO3 = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)

\(1.a.CaCO_3.t^o\rightarrow CaO+CO_2\\ b.m_{CaCO_3}=m_{CaO}+m_{CO_2}\\ \Rightarrow m_{CO_2}=m_{CaCO_3}-m_{CaO}=20-11,2=8,8\left(g\right)\)

\(n_{CaCO_3}=\dfrac{m_{CaCO_3}}{M_{CaCO_3}}=\dfrac{4000}{100}=40mol\)
\(n_{CaO}=\dfrac{m_{CaO}}{M_{CaO}}=\dfrac{1680}{56}=30mol\)
\(CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\)
40 30 ( mol )
30 30
\(H=\dfrac{30}{40}.100=75\%\)

PTPƯ:
\(CaCO_3\underrightarrow{t^o}CaO+CO_2\)\(\uparrow\)
0,015 0,015 0,015
\(nCaCO_3=\dfrac{1,5}{100}=0,015mol\)
\(mCaO=0,015.56=0,84\)(tấn)
Đổi: \(7\) \(tấn\) = \(7000000\) \(g\)
Phương trình hóa học:
\(CaCO_3\rarr CaO+CO_2\)
Tỉ lệ số \(mol\): \(1:1:1\)
\(\) \(\rArr1\) \(mol\) \(CaCO_3\) phản ứng tạo ra \(1\) \(mol\) \(CaO\)
\(\rArr1\) \(mol\) \(CaCO_3\) phản ứng tạo ra \(1\) \(mol\) \(CO_2\)
\(nCaO=\frac{7000000}{\left(40+16\right)}=\frac{7000000}{56}=125000\left(mol\right)\)
\(\rArr nCaCO_3=nCaO=nCO_2=125000\) \(mol\)
\(\rArr mCaCO_3=125000\times\left(40+12+16\times3\right)=125000\times100=12500000\) \(\left(g\right)=12,5\) \(\left(tấn\right)\)
\(\rArr\) Lượng quặng đá vôi cần dùng là: \(\frac{12,5}{80\%}=15,625\left(tấn\right)\)
\(\rArr nCO_2=125000\times\left(12+16\times2\right)=125000\times44=5500000\left(g\right)=5500\left(\operatorname{kg}\right)\)
Vậy cần dùng \(15,625\) \(tấn\) quặng đá vôi, tạo ra \(5500\operatorname{kg}\) khí \(CO_2\)