Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) KClO3 + 6HCl --> KCl + 3Cl2 + 3H2O
Chất khử: HCl, chất oxh: KClO3
| QT khử | Cl+5 + 6e --> Cl-1 | x1 |
| QT oxh | 2Cl-1 - 2e --> Cl20 | x3 |
b) 2KMnO4 --to--> K2MnO4 + MnO2 + O2
Chất khử: KMnO4, chất oxh: KMnO4
| QT khử | 2Mn+7 + 4e --> Mn+6 + Mn+4 | x1 |
| QT oxh | 2O-2 - 4e --> O20 | x1 |
\(a.QToxh:2\overset{-1}{Cl}\rightarrow Cl_2+2e|\times5\\QTkhử:2\overset{+5}{Cl}+10e\rightarrow \overset{0}{Cl_2}|\times1\)
HCl là chất oxi hóa, KClO3 là chất khử
\(KClO_3+6HCl_{đặc}\rightarrow KCl+3Cl_2+3H_2O\)
\(b.QToxh:2\overset{-2}{O}\rightarrow\overset{0}{O_2}+4e|\times1\\ QTkhử:2\overset{+7}{Mn}+4e\rightarrow\overset{+6}{Mn}+\overset{+4}{Mn}|\times1\)
KMnO4 vừa là chất khử, vừa là chất oxi hóa
\(2KMnO_4-^{t^o}\rightarrow K_2MnO_4+MnO_2+O_2\)

A. 2KClO3 -> 2KCl + O2
B. Na2O + H2O -> 2NaOH
C. 3Fe + 2O2 -> Fe3O4
D. 2HgO -> 2Hg + o2
E. O2 + 2H2 -> 2H2O
G.2 KMnO4 -> K2MnO4 + MnO2 + O2
H. 2SO2 + O2 ->2 SO3
Bạn k biết cân bằng à..Sao đăng nhiều vayaja...Toàn đagư mấy câu cân bằng..Có câu còn lặp lại nữa

1) \(Fe^0+H_2S^{+6}O_4\rightarrow Fe^{+3}_2\left(SO_4\right)_3+S^{+4}O_2+H_2O\)
Có:\(\left\{{}\begin{matrix}1\times|2Fe^0\rightarrow Fe_2^{+3}+6e\left(1\right)\\3\times|S^{+6}+2e\rightarrow S^{+4}\left(2\right)\end{matrix}\right.\)
\(\Rightarrow2Fe+6H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
Chất khử: H2SO4; chất oxi hóa:Fe; quá trình (1) là quá trình oxi hóa và quá trình (2) là quá trình khử
2)\(KMn^{-7}O_4\rightarrow K_2Mn^{-6}O_4+Mn^{-4}O_2+O_2\)
Có:\(\left\{{}\begin{matrix}1\times|2Mn^{+7}+4e\rightarrow Mn^{+6}+Mn^{+4}\left(1\right)\\1\times|2O_4^{-2}\rightarrow O^{-2}_4+O^{-2}_2+4e\left(2\right)\end{matrix}\right.\)
\(\Rightarrow2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
KMnO4 vừa là chất khử, vừa là chất oxi hóa. Quá trình (2) là quá trình oxi hóa, (1) là quá trình khử
3)\(KCl^{+5}O_3^{-2}\rightarrow KCl^{-1}+O_2\)
Có\(\left\{{}\begin{matrix}3\times|2O^{-2}\rightarrow O^0_2+4e\left(1\right)\\2\times|Cl^{+5}+6e\rightarrow Cl^{-1}\left(2\right)\end{matrix}\right.\)
\(\Rightarrow2KClO_3\rightarrow2KCl+3O_2\)
KClO3 vừa là chất khử, vừa là chất oxi hóa. Quá trình (1) là quá trình oxi hóa, (2) là quá trình khử
4)\(Al^0+Fe^{+\frac{8}{3}}_3O_4\rightarrow Al^{+3}_2O_3+Fe^0\)
Có\(\left\{{}\begin{matrix}3\times|3Fe^{+\frac{8}{3}}+8e\rightarrow Fe^0\left(1\right)\\8\times|Al^0\rightarrow Al^{+3}+3e\left(2\right)\end{matrix}\right.\)
\(\Rightarrow8Al+3Fe_3O_4\rightarrow4Al_2O_3+9Fe\)
Fe3O4 là chất khử và Al là chất oxi hóa. Quá trình (1) là quá trình khử và quá trình (2) là quá trình oxi hóa
5)\(Cl^0_2+K^{+1}OH\rightarrow KCl^{-1}+KCl^{+5}O_3+H_2O\)
Có:\(\left\{{}\begin{matrix}1\times|Cl^0\rightarrow Cl^{+5}+5e\left(1\right)\\5\times|Cl^0+e\rightarrow Cl^{-1}\left(2\right)\end{matrix}\right.\)
\(\Rightarrow3Cl_2+6KOH\rightarrow KCl+5KClO_3+3H_2O\)
Cl2 vừa là chất khử, vừa là chất oxi hóa. Quá trình (1) là quá trình khử, quá trình (2) là quá trình oxi hóa

Đáp án A
Các phương trình phản ứng:
Nhiệt phân hỗn hợp X:
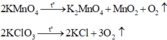
Chất rắn Y gồm K2MnO4, MnO2, KCl, KMnO4 dư. Rắn Y tác dụng với dung dịch HCl đặc:
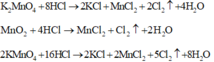
Tính toán:
Gọi số mol các chất trong hỗn hợp X là KMnO4: a mol ; KClO3: b mol. Ta có:
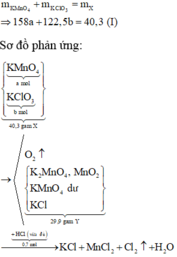
Bảo toàn khối lượng cho giai đoạn nhiệt phân X ta có:
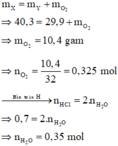
Theo sơ đồ thì cuối cùng O trong Y chuyển hết về H2O. Bảo toàn nguyên tố O cho giai đoạn nhiệt phân X ta có:

Xét giai đoạn nhiệt phân X:
Gọi x là số mol KMnO4 phản ứng
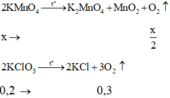
Hiệu suất nhiệt phân KMnO4 là:
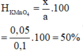

30,005 gam X gồm x mol KMnO4 + y mol KClO3 và z mol MnO2 .
\(m_X=158x+122,5y+87z=30,005\left(g\right)\)
\(n_{HCl\left(cd\right)}=0,8\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{O\left(trong.Y\right)}=0,4\left(mol\right)\\n_{O\left(thoat.ra\right)}=\frac{30,005-24,405}{32}=0,175\left(mol\right)\end{matrix}\right.\)
Bảo toàn O có:
\(4a+3y+2z=0,175.2+0,4=0,75\left(mol\right)\)
Bảo toàn electron cả quá trình có:
\(5x+6y+2z=4n_{O2}+2n_{Cl2}=1,1325\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,12\left(mol\right)\\y=0,0875\left(mol\right)\\z=0,00375\left(mol\right)\end{matrix}\right.\)
MnO2 không nhiệt phân; ở đây dùng một lượng ít này cảm giác như là xúc tác
Cho 0,0875 mol KClO3 nhiệt phân hoàn toàn tạo 0,13125 mol O2 .
→ Còn cần 0,0875 mol KMnO4 phản ứng nhiệt phân nữa để tạo thêm 0,04375 mol O2
\(\Rightarrow\%_{KMnO4\left(bi.nhiet.phan\right)}=\frac{0,0875}{12}.100\%=72,92\%\)
2 KMnO4---> K2MnO4+MnO2+O2
Mn(+7) +3e --->Mn(+4)
Mn (+7) +1e--->Mn(+6)
O(-2) ----> O(0) +2e
4KMnO4 ----> 2MnO2 + 2K2MnO4 +2O2