
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


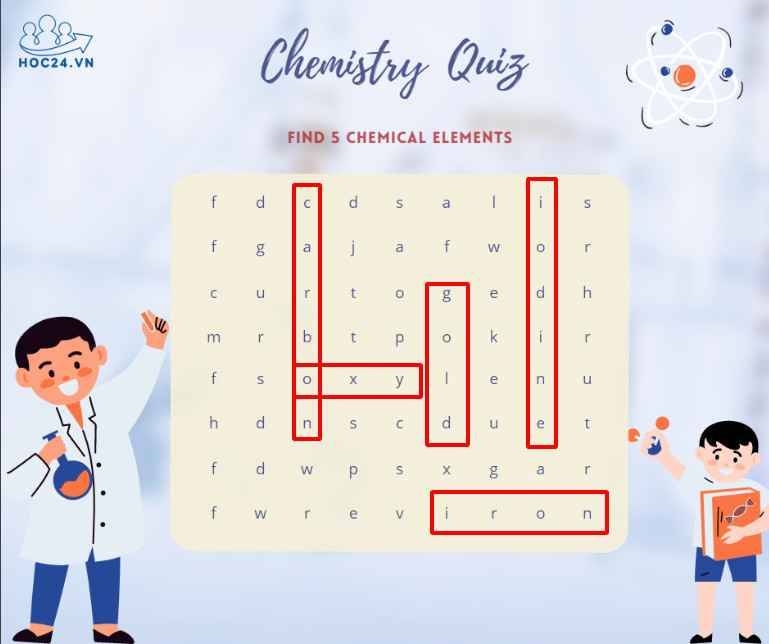
*cái oxy em k chắc á cô:<< em tìm được mấy nguyên tố này th ạ:<.


Câu 3:
N2+O2\(\overset{t^0}{\rightarrow}\)2NO
4NO+3O2+2H2O\(\rightarrow\)4HNO3
NO3- : làm tăng lượng phân đạm cho cây!

a;Zn + 2HCl\(\rightarrow\)ZnCl2+H2
Zn+ H2SO4\(\rightarrow\)ZnSO4+H2
b;TN1:
\(\sum n_{H_2}=0,1+0,1=0,2\left(mol\right)\)
VH2=22,4.0,2=4,48(lít)
TN2:
\(\sum n_{H_2}=0,1+0,05=0,15\left(mol\right)\)
VH2=22,4.0,15=3,36(lít)
Vậy ở TN1 sinh ra nhiều H2 hơn

1. a) Tên gọi của axit:
HNO3: axit nitric
HCl: axit clohidric
H2CO3: axit cacbonic
H2S: axit sunfuhidric
H2SO4: axit sunfuric
H2SO3: axit sunfurơ
Axit mạnh: HCl, HNO3, H2SO4...
Axit yếu: H2S, H2CO3...



Em có thể hỏi bạn Trần Hữu Tuyển. Cô đã chữa cho bạn ấy đề này rồi
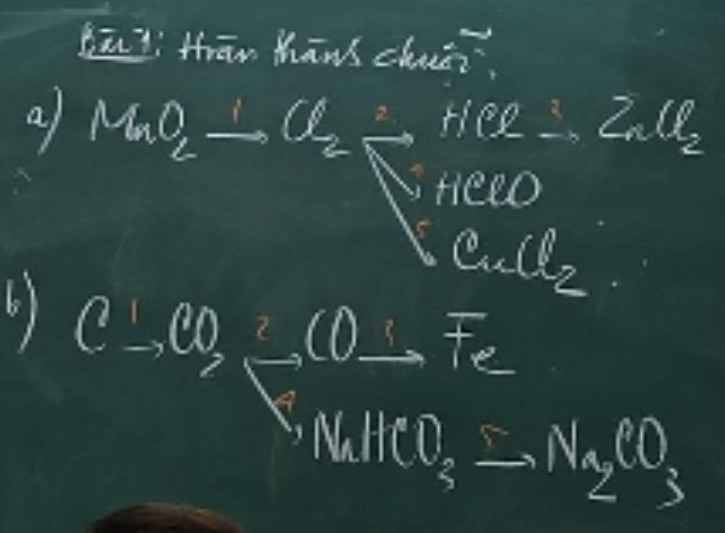
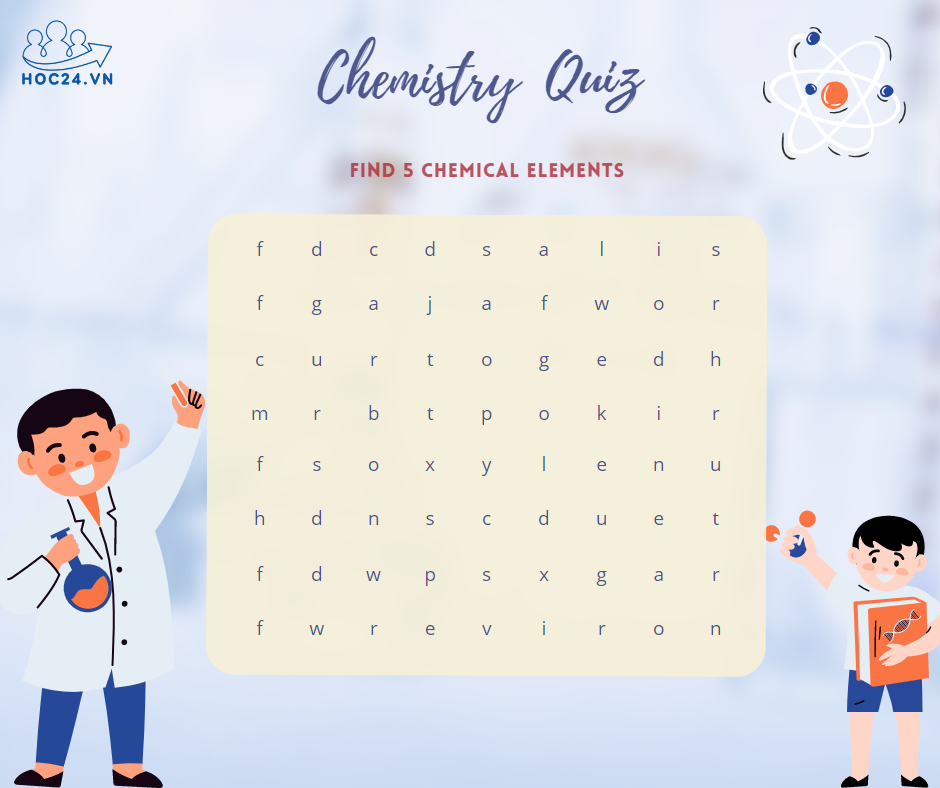
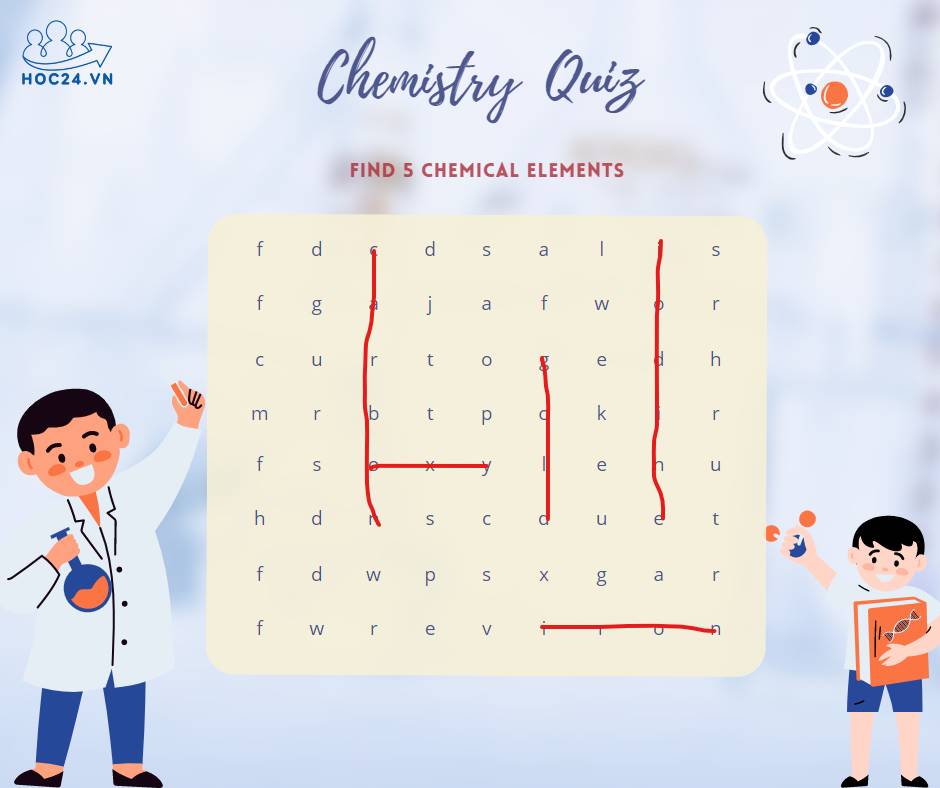

 mn giúp e những câu còn lại ạ :)
mn giúp e những câu còn lại ạ :)










 Giúp mình giải vài câu thực tế Hoá nha..
Giúp mình giải vài câu thực tế Hoá nha..





 Bài 5.5 ạ
Bài 5.5 ạ
 Giúp hộ mình nha !!!
Giúp hộ mình nha !!! Cảm ơn bạn !!!
Cảm ơn bạn !!!




 chọn đáp án ạ
chọn đáp án ạ
a, (1) \(MnO_2+4HCl\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O\)
(2) \(Cl_2+H_2\rightarrow2HCl\)
(3) \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
(4) \(Cl_2+H_2O⇌HCl+HClO\)
(5) \(Cu+Cl_2\underrightarrow{t^o}CuCl_2\)
b, (1) \(C+O_2\underrightarrow{t^o}CO_2\)
(2) \(CO_2+C\underrightarrow{t^o}2CO\)
(3) \(3CO+Fe_2O_3\underrightarrow{t^o}2Fe+3CO_2\)
(4) \(CO_2+NaOH\rightarrow NaHCO_3+H_2O\)
(5) \(NaHCO_3+NaOH\rightarrow Na_2CO_3+H_2O\)
a)
\(\left(1\right)MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
\(\left(2\right)Cl_2+H_2O\rightarrow HCl+HClO\)
\(\left(3\right)Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(\left(4\right)Cl_2+H_2O\rightarrow HCl+HClO\)
\(\left(5\right)Cu+Cl_2\rightarrow CuCl_2\)
b)
\(\left(1\right)C+O_2\rightarrow CO_2\)
\(\left(2\right)CO_2+C\rightarrow2CO\)
\(\left(3\right)Fe_3O_4+4CO\rightarrow3Fe+CO_2\)
\(\left(4\right)CO_2+NaOH\rightarrow NaHCO_3\)
\(\left(5\right)NaHCO_3+NaOH\rightarrow Na_2CO_3+H_2O\)