Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

TL:
Điện hóa trị của Cs là 1+, Cl là 1-; Na là 1+, O là 2-; Ba là 2+, Al là 3+

F O Cl N
Độ âm điện: 3,98 3,44 3,16 3,14
Nhận xét: tính phi kim giảm dần.
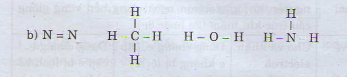
N2 CH4 H2O NH3
Hiệu độ âm điện: 0 0,35 1,24 0,84
Phân tử N2, CH4 có liên kết cộng hóa trị không phân cực. Phân tử H2O có liên kết cộng hóa trị phân cực mạnh nhất trong dãy.

H2O: H+1 ; O-2
H2S: H+1; S-2
OF2: O:-2; F+1
H2O2: H+1; O -1 (TH đặc biệt)
NaOH: Na+1; O-2l H+1
MgCl2: Mg+2; Cl-1

Lấy giá trị độ âm điện của các nguyên tố ở bảng 6 trang 45
Hiệu dộ âm điện CaCl2 : 2, 16 -> Liên kết ion.
Hiệu độ âm điện AlCl3, CaS, Al2S3 lần lượt là : 1,55 ; 1,58 ; 0,97 -> Liên kết cộng hóa trị có cực.
a) Dựa vào số hiệu nguyên tử của mỗi ng tử ở trên, viết CHe ra.
Ta xét: nguyên tử nào có e lớp ngoài cùng dạng \(ns^xnp^y\)
Nếu \(\left[{}\begin{matrix}x+y=1\\x+y=2\\x+y=3\end{matrix}\right.\)thì là kim loại ( trừ H(Z = 1); He(Z=2); B(Z=5))
Hoặc e ngoai cũng có dạng \(\left(n-1\right)d^xns^y\)\(\Rightarrow KL\)
b) Dựa vào định nghĩa nguyên tố s, p, d, f trong SGK => ta xác định được.
Để làm được câu b thì em phải viết cấu hình e.