Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

X: Fe3O4
Y: FeCl2
Z: FeCl3
T: Fe(OH)2
U: Fe(OH)3
A: NaCl (hoặc H2O)
B: H2O (hoặc NaCl)
D: H2 (hoặc Cl2)
E: Cl2 (hoặc H2)
F: NaOH
G: HCl
PTHH:
a) NaCl + H2O -dpmn----> 1/2 H2 + 1/2 Cl2 + NaOH
H2 + Cl2 -to-> 2 HCl
HCl + NaOH -> NaCl + H2O
b) 3 Fe +2 O2 -to->Fe3O4
Fe3O4 + 8 HCl -> FeCl2 +2 FeCl3 + H2O
FeCl2 + 2 NaOH -> Fe(OH)2 + 2 NaCl
FeCl3 +3 NaOH -> Fe(OH)3 + 3NaCl
Chúc em học tốt!

$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O(1)$
$Fe_2(SO_4)_3 + Fe\ to 3FeSO_4(2)$
Gọi $n_{Fe_2(SO_4)_3} = a(mol) ; n_{FeSO_4} = b(mol)$
Ta có : $400a + 152b = 62,8(1)$
$n_{SO_2} = 0,15(mol)$
$n_{Fe_2(SO_4)_3(1)} = \dfrac{1}{3}n_{SO_2} = 0,05(mol)$
$n_{Fe_2(SO_4)_3(2)} = \dfrac{1}{3}n_{FeSO_4} = \dfrac{b}{3}$
Suy ra:
$0,05 - \dfrac{b}{3} = a(2)$
Từ (1)(2) suy ra $a = \dfrac{45}{112} ; b = -1,055<0$
=> Sai đề

\(n_{HCl}=\dfrac{7,3\%.b}{100\%.36,5}=0,002b\left(mol\right)\)
\(MgO+2HCl--->MgCl_2+H_2O\)
0,002b..............................0,002b
\(a+27,5=0,002.b.95\)
\(\Leftrightarrow0,002.b.40+27,5=0,19.b\)
\(\Leftrightarrow0,08b+27,5=0,19.b\)
\(\Leftrightarrow b=250\)
\(a=40.0,002.250=20\)
\(m_{MgCl_2}=20+27,5=47,5\left(g\right)\)
\(C\%=\dfrac{47,5}{20+250}.100\%\approx17,59\%\)
nhưng mà số mol của MgCl2 bằng 1/2 số mol của HCl
nên số mol của MgCl2 = 0.002/2 = 0.001 chứ

Bạn tự viết PTHH nhé.
a)nNaOH=0.025mol
Từ PTHH->nH+p/u với NaOH=nNaOH=2.025mol
Đặt nH2SO4=amol.->nHCl=3amol
->nH+ trong dd=2a+3a=5a mol
->a=0.01
->nHCl=0.03mol;nH2SO4=0.01mol
b)nHCl=0.06mol;nH2SO4=0.02mol
->nH+=0.06+0.02x2=0.1mol
->nOH- có thể p/u=nH+=0.1mol
Đặt VddB=x(l)
->nNaOH=0.2xmol;nBa(OH)2=xmol
->nOH-=0.2x+2x=2.2xmol
->x=0.025(l)
c)Áp dụng DLBTKL
->m muối=m axit +m bazo -m H2O
n H2O=1/2 nH+=0.05mol<=>0.9g
->m muối=0.06x36.5+0.02x98+0.2x0.025x40+
0.025x171-0.9=7.725g
Mình nghĩ chắc là đúng rồi đó.

CaO + 2HCl -> CaCl2 + H2O
nCaO=0,02(mol)
nHCl=\(\dfrac{500.3,65\%}{36,5}=0,5\left(mol\right)\)
Vì 0,02.2<0,5 nên HCl dư 0,46(mol)
Theo PTHH ta có:
nCaO=nCaCl2=0,02(mol)
mCaCl2=111.0,02=2,22(g)
mHCl=0,46.36,5=16,79(g)
C% dd HCl dư=\(\dfrac{16,79}{500+1,12}.100\%=3,35\%\)
C% dd CaCl2=\(\dfrac{2,22}{500+1,12}.100\%=0,443\%\)

\(n_{HCl}=\dfrac{V}{22,4}=\dfrac{5,6}{22,4}=0,25mol\)
\(m_{HCl}=n.M=0,25.36,5=9,125g\)
\(C_{M_{HCl}}=\dfrac{n}{V}=\dfrac{0,25}{0,1}=2,5M\)
mdd=v.d=mH2O=0,1.1000.1=100g
\(C\%_{HCl}=\dfrac{m_{HCl}.100}{m_{dd}}=\dfrac{9,125.100}{100}=9,125\%\)


https://hoc24.vn/hoi-dap/question/71825.html bạn vào đây tham khảo nè




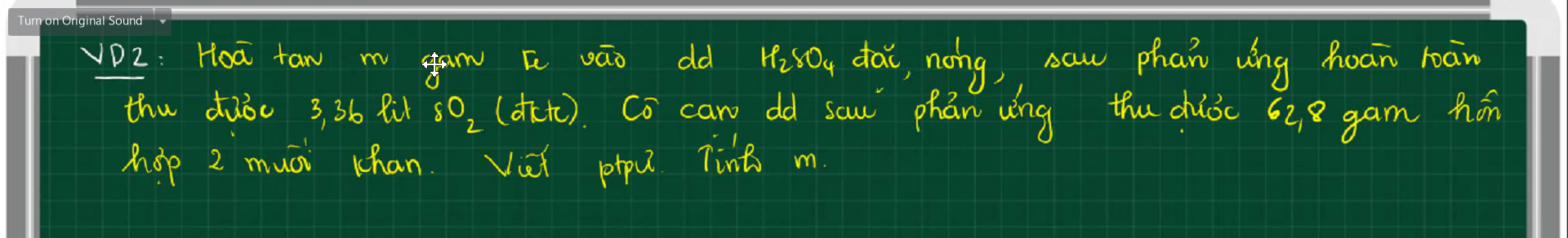
 Giúp hộ mình nha !!!
Giúp hộ mình nha !!!