Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án: D
Gọi số mol axit và ancol trong mỗi phần lần lượt là x và y.
CH3COOH + K → 1 / 2 H 2
C2H5OH + K → 1 / 2 H 2
=> x + y = 0,15
CH3COOH + Na2CO3 → CH3COONa + CO2 + H2O
=> y = nCO2 = 0,05
=> => Khi este hóa, ancol phản ứng hết (theo lí thuyết)
Vì hiệu suất là 60% => n este = 0,6.0,1 = 0,06 mol
=> meste = 0,06.88 = 5,28g

Đáp án B
2Cu(NO3)2 → t o 2CuO + 4NO2 + O2
Do chất rắn thu được + HNO3 giải phóng khí NO => Cu dư => O2 sinh ra do phản ứng nhiệt phân phản ứng hết với Cu
=> mrắn giảm = mNO2 bay lên= 9,2 (g) => nNO2 =0,2 (mol)
BTNT N => nCu(NO3)2 = ½ nNO2 = 0,1 (mol)
=> % mCu = 31,6 – 0,1.188 = 12,8 (g)

Đáp án C
Xử lí dữ kiện Z: Bảo toàn khối lượng:
![]() = 6,12 gam
= 6,12 gam
→![]() gam →
gam →
![]() mol
mol
→ ![]() gam →
gam →
![]() mol.
mol.
![]()
![]() gam
gam
![]() mol
mol
![]()
![]()
Ta có phản ứng Dumas: -COONa + NaOH → -H + Na2CO3 (vôi tôi xút).
![]()
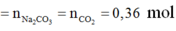
![]()
![]()
K gồm 2 khí trong đó có CH4.
Mà sau khi dẫn qua dung dịch Br2 dư chỉ còn 1 khí thoát ra
⇒ khí còn lại bị hấp thụ.
![]()
trong A chứa 2 gốc CH3COO-
⇒ gốc còn lại cũng là gốc axit đơn chức
⇒ nkhí còn lại = nA = 0,12 mol.
⇒ Mkhí còn lại =
![]()
khí còn lại là C2H4.
⇒ là (CH3COO)2(CH2=CH-COO)C3H5
⇒ a = 0,12 . 230 = 2,76
![]() mol
mol
⇒ x = 0,38 ÷ 0,19 = 2.
Muối gồm 0,12 mol
![]() ;
;
0,24 mol CH3COONa; 0,02 mol NaCl
=> b = 0,12.94 + 0,24.82 + 0,02.58,5 = 32,13
=> a + b + x = 61,73 gam

Đáp án A
Ta có sơ đồ phản ứng:
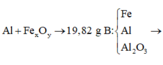
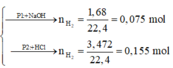
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
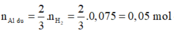
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
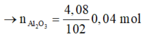
Ta có:
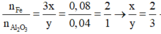
=> Oxit sắt cần tìm là Fe2O3

Khối lượng bình tăng chính là khối lượng C O 2 và H 2 O suy ra m C O 2 + m H 2 O = 74 , 225 g a m
Khối lượng dung dịch giảm bằng m d d g i ả m = m B a C O 3 - ( m C O 2 + m H 2 O ) = 161 , 19 g a m
→ m B a C O 3 = 235 , 415 g a m → n C O 2 = 1 , 195 m o l → n H 2 O = 1 , 2025 m o l
Quy đổi Z thành: C 2 H 3 O N a m o l , C H 2 b m o l v à H 2 O c m o l
Bảo toàn nguyên tố C ta có 2a + b = n C O 2 = 1 , 195 m o l 1
Bảo toàn nguyên tố H ta có 1,5a + b + c = n H 2 O = 1 , 2025 m o l 2
139,608 lít khí trơ thoát ra chính là khí N 2 . Suy ra n N 2 = 6 , 2325 m o l
Bảo toàn nguyên tố O ta có: n O 2 = ( 2. n C O 2 + n H 2 O − a − c ) / 2 = 3 , 5925 − a − c / 2
Suy ra số mol N 2 trong không khí bằng n N 2 ( t r o n g k h ô n g k h í ) = 4 . n O 2 = 2 . ( 3 , 5925 - a - c )
Tổng số mol N 2 thu được bằng n N 2 ( t ổ n g ) = a / 2 + 2 . ( 3 , 5925 - a - c ) = 6 , 2325 ( 3 )
Giải hệ (1), (2), (3) ta có a = 0,375; b = 0,445; c = 0,195
Y tác dụng với KOH:
Một nửa hỗn hợp Z phản ứng: Z + KOH → Muối + H 2 O
Ta có số mol KOH phản ứng với Z bằng a = 0,375 mol
Ta có: n H 2 O = n Z = c = 0 , 195 m o l ; m Z = 31 , 115 g a m
Bảo toàn khối lượng ta có: m m u o i = 48 , 605 g a m
Vậy nếu toàn bộ Z phản ứng thì số mol KOH phản ứng với Z bằng 0,75 mol và m m u ố i = 97 , 21 g a m
Ta có: n H 2 S O 4 = 0 , 5 m o l → n K O H = 1 m o l v à m K 2 S O 4 = 87 g a m
Số mol KOH phản ứng tổng = 1 , 75 m o l → n K O H d ư = 0 , 35 m o l → m K O H d ư = 19 , 6 g a m
Khi cho Y tác dụng với KOH thì thu được 97,21 gam muối + K 2 S O 4 0 , 5 m o l + KOH dư (0,35 mol)
Vậy khối lượng chất rắn bằng 97,21 + 87 + 19,6 = 203,81 (gam)
Khối lượng chất rắn có giá trị gần đúng là 204 gam
Đáp án cần chọn là: B
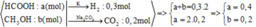
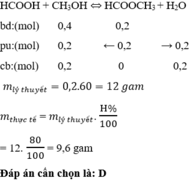


nZn=\(\dfrac{m}{M}=\dfrac{12,8}{65}=0,197\left(mol\right)\)
pthh:
Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
0,197..0,394.....0,197...0,197(mol)
2H2 + O2 \(\rightarrow\) 2H2O
0,197................0,197
mH2O=n.M=0,197.18=3,546(g)