Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 1 :
Khối lượng FeS thu được sau phản ứng biết lưu huỳnh dư 1,6 g :
mFe = mFe + mS - mS.dư
= 2,8 + 3,2 - 1,6
= 4,4 (g)

Gọi x(g là khối lượng vỏ Trái đất).
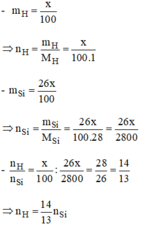
Vậy số nguyên tử của hidro nhiều hơn số nguyên tử của sillic

X là kim loại phổ biến nhất trên Trái Đất ---> X là Al
Z là phi kim phổ biến nhất trên Trái Đất ---> Z là O
Ta có: \(\left\{{}\begin{matrix}\%Z=2.\%Y\\\%Y+\%Z+15,79\%=100\%\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}\%Z=56,14\%\\\%Y=28,07\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_{Al}=342.15,79\%=54\left(g\right)\\m_O=56,14\%.342=192\left(g\right)\\m_Y=342-54-192=96\left(g\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}n_{Al}=\dfrac{54}{27}=2\left(mol\right)\\n_O=\dfrac{192}{16}=12\left(mol\right)\\n_Y=\dfrac{96}{M_Y}=k\left(mol\right)\left(đk:k\in N\text{*}\right)\end{matrix}\right.\)
CTHH là \(Al_2O_{12}Y_k\)
Vì tổng số oxi hoá của hợp chất luôn bằng không nên: (gọi số oxi hoá của Y là a)
\(2.\left(+3\right)+12.\left(-2\right)+ak=0\\ \Leftrightarrow ak-18=0\\ \Leftrightarrow ak=18\)
Hay \(a.\dfrac{96}{M_Y}=18\Leftrightarrow M_Y=\dfrac{16}{3}a\)
Vì a là số oxi hoá nên ta xét bảng
| a | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| MY | \(\dfrac{16}{3}\) | \(\dfrac{32}{3}\) | 16 | \(\dfrac{64}{3}\) | \(\dfrac{80}{3}\) | 32 | \(\dfrac{112}{3}\) |
| Loại | Loại | Loại | Loại | Loại | S (lưu huỳnh) | Loại |
\(\rightarrow k=\dfrac{96}{M_S}=\dfrac{96}{32}=3\left(TM\right)\)
CTHH là \(Al_2S_3O_{12}\) hay \(Al_2\left(SO_4\right)_3\)

a/ Khối lượng chất rắn sẽ giảm đi vì sau khi ngung sẽ có khi thoát ra ( bay đi)
PTHH CaCO3 =(nhiệt)==> CaO + CO2\(\uparrow\)
b/ Khối lượng chất rắn sẽ tăng lên vì
Áp dụng định luật bảo toàn khối lượng
mCu + mO2 = mCuO > mCu
c+ d/ Tương tự phần b nhé
a) Nung nóng có nghĩa là hiện tượng này bị nhiệt phân nên khối lượng vật rắn giản so với ban đầu.

1) nFe3O4= 46,4:232=0,2 mol
PTHH :3Fe+2O2\(\rightarrow\) Fe3O4
0,6 0,4 \(\leftarrow\)0,2 (mol)
PTHH: 2KMnO4\(\rightarrow\) K2MnO4+MnO2+O2
0,8 \(\leftarrow\) 0,4 (mol)
\(\Rightarrow\) m KMnO4= 0,8.158=126,4 g
1) 3Fe + 2O2 ---> Fe3O4 ---> nO2 = 2nFe3O4 = 2.46,4/232 = 0,4 mol.
2KMnO4 ---> K2MnO4 + MnO2 + O2 ---> nKMnO4 = 2nO2 = 0,8 mol
---> mKMnO4 = 158.0,8 = 126,4 g.
2) KClO3 ---> KCl + 3/2O2 ---> nKClO3 = 2/3nO2
---> nKClO3:nKMnO4 = 2/3:2 = 1:3 ---> mKClO3:mKMnO4 = 158/3.122,5 = 0,43
3) KNO3 ---> KNO2 + 1/2O2 ; Cu(NO3)2 ---> CuO + 2NO2 + 1/2O2
Như vậy nếu thu được cùng lượng oxi thì KClO3 sẽ có khối lượng nhỏ nhất.

a. Trong 1 mol Cu(NO3)2 có:
- 1 mol Cu
- 2 mol N
- 6 mol O
b. mCu = 1 x 64 = 64 gam
mN = 2 x 14 = 28 gam
nO = 6 x 16 = 96 gam
c. nCu(NO3)2 = 37,6 / 188 = 0,2 mol
=> nCu = 0,2 mol
nN = 0,2 x 2 = 0,4 mol
nO = 0,2 x 6 = 1,2 mol
=> mCu = 0,2 x 64 = 12,8 gam
mN = 0,4 x 14 = 5,6 gam
mO = 1,2 x 16 = 19,2 gam
SAI MÔN KÌA