Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Các đồng phân hydrocarbon thơm có công thức phân tử C8H10:
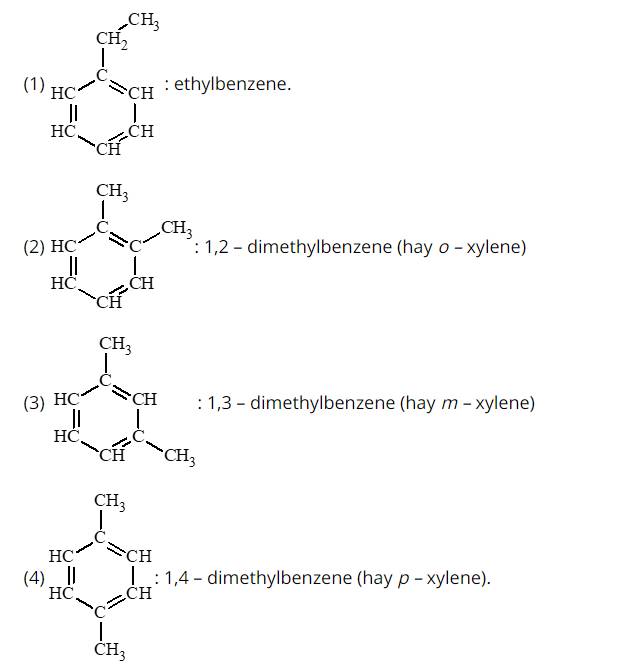
Chất (3) và (4) là đồng phân về số lượng các gốc alkyl gắn với vòng benzene của o – xylene.

- Arene là những hydrocarbon có chứa vòng benzene trong phân tử.
- Cấu tạo: Hydrocarbon chứa vòng benzene.
- Tính chất:
+ Tính chất vật lí: Các arene đều độc, không tan trong nước, tan nhiều trong các dung môi hữu cơ. Một số arene có mùi đặc trưng.
+ Tính chất hóa học: Arene tham gia phản ứng thế, phản ứng cộng, phản ứng oxi hóa.
- Ứng dụng:
+ Toluene còn là dung môi và chất trung gian trong quá trình sản xuất các loại hoá chất khác;
+ p−xylene là nguyên liệu sản xuất tơ polyester; benzene dùng trong sản xuất phẩm nhuộm, dược phẩm, chất tẩy rửa;
+ styrene dùng để sản xuất polystyrene, một chất dẻo đa dụng trong cuộc sống.

Tham khảo:
Trong phân tử phenol, nhóm –OH liên kết trực tiếp với vòng benzene. Chính nhờ có sự liên kết này, vòng benzene trở thành nhóm hút electron, làm giảm mật độ electron ở nguyên tử oxygen và tăng sự phân cực của liên kết O–H (so với trong phân tử alcohol); đồng thời làm tăng mật độ electron trong vòng benzene, nhất là ở các vị trí ortho và para.
=> Phenol có phản ứng thế nguyên tử H ở nhóm –OH (thể hiện tính acid) và phản ứng thế nguyên tử H của vòng benzene.

Đặc điểm cấu tạo phân tử benzene:
+ Gồm 6 nguyên tử H và 6 nguyên tử C nằm trong cùng một mặt phẳng.
+ 6 nguyên tử C tạo thành hình lục giác đều, mỗi nguyên tử C lại liên kết với một nguyên tử H nữa.
+ Độ dài các liên kết C-C bằng nhau, độ dài các liên kết C-H cũng như nhau.
- Trong phân tử benzene có vòng benzene, khác so với các hydrocarbon đã học.

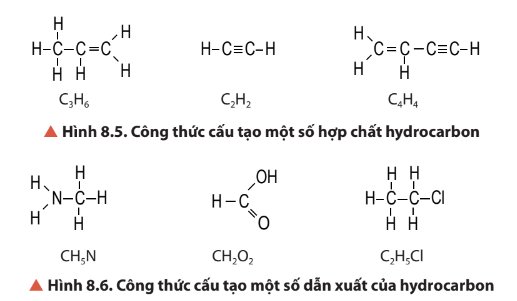
Thành phần nguyên tố của hydrocarbon trong Hình 8.5 là carbon và hydrogen.
Thành phần nguyên tố trong dẫn xuất của hydrocarbon trong Hình 8.6: ngoài carbon và hydrogen, còn có các nguyên tố khác như nitrogen, oxygen, chlorine.

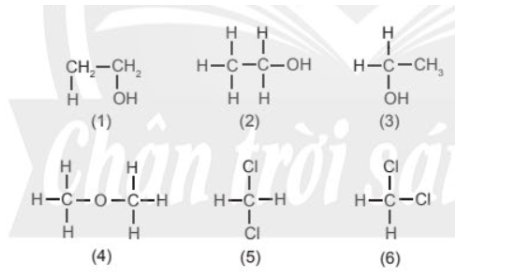
(1), (2), (3) cùng 1 chất: Rượu etylic (CH3-CH2-OH)
(5), (6) cùng 1 chất (CH2Cl2)

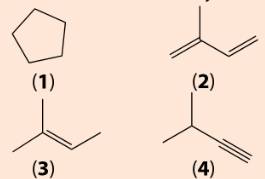
Công thức phân tử của các chất, nhận biết các chất :
1. C6H12 - Alkane
2. C5H8 - Alkane
3. C5H10 - Alkane
4. C5H8 - Alkane

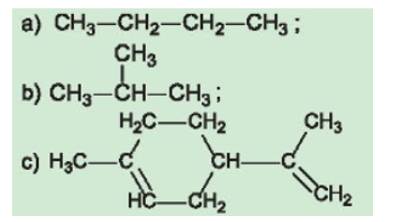
a) Mạch hở không phân nhánh;
b) Mạch hở phân nhánh;
c) Mạch vòng, có nhánh.
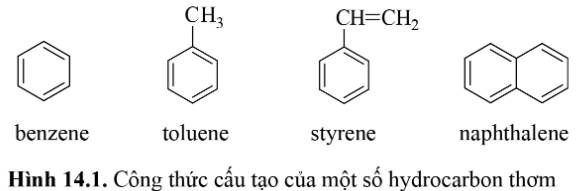

- Giống nhau: hydrocarbon thơm, alkane và alkene đều được cấu tạo bởi nguyên tố C và nguyên tố H.
- Khác nhau:
+ Hydrocarbon thơm có vòng benzene.
+ Alkane và alkene là những hydrocarbon mạch hở, không có vòng benzene.