Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. Cho dd phenolphtalein vào các mẫu thử đã trích:
+ Hồng: KOH
+ Không đổi màu: KCl, H2SO4
Cho dd KOH đã tìm được vào nhóm k đổi màu:
+ Không hiện tượng: KCl
+ Có chất rắn mới: H2SO4

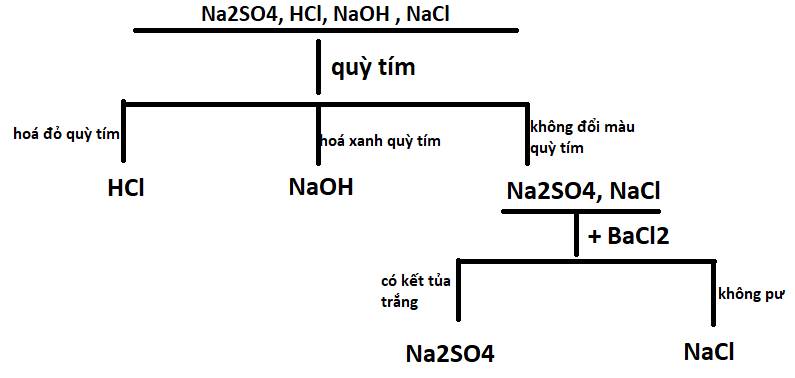
Trích mẫu thử
Cho quỳ tím vào mẫu thử
- mẫu thử làm quỳ tím hóa đỏ là HCl
- mẫu thử làm quỳ tím hóa xanh là NaOH
Cho dung dịch $BaCl_2$ vào hai mẫu thử còn :
- mẫu thử tạo kết tủa trắng là $Na_2SO_4$
$Na_2SO_4 + BaCl_2 \to BaSO_4 + 2NaCl$
- mẫu thử không hiện tượng là NaCl

- Cho các dd tác dụng với quỳ tím
+ QT chuyển xanh: NaOH
+ QT chuyển đỏ: HCl
+ QT không chuyển màu: NaNO3, NaCl
- Cho 2 dd còn lại tác dụng với dd AgNO3
+ Kết tủa trắng: NaCl
NaCl + AgNO3 --> AgCl\(\downarrow\) + NaNO3
+ Không hiện tượng: NaNO3

a)
Cho quỳ tím vào
+ chuyển đỏ HCl, H2So4
+ không chuyển màu K2So4
Cho dd BaCl2 vào nhóm chuyển đỏ xh kết tủa là H2So4
PT
H2So4+2BaCl2->BaSo4+HCl
+ còn lại HCl không hiện tượng
b)
- Dùng quỳ tím
+) Hóa đỏ: HCl, H2SO4 và HNO3
+) Hóa xanh: KOH
- Đổ dd BaCl2 vào 3 dd trên
+) Xuất hiện kết tủa: H2SO4
PTHH: \(BaCl_2+H_2SO_4\rightarrow2HCl+BaSO_4\downarrow\)
+) Không hiện tượng: HNO3 và HCl
- Đổ dd AgNO3 vào 2 dd còn lại
+) Xuất hiện kết tủa: HCl
PTHH: \(AgNO_3+HCl\rightarrow HNO_3+AgCl\downarrow\)
+) Không hiện tượng: HNO3

a, - Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa đỏ: HCl, H2SO4. (1)
+ Quỳ không đổi màu: Na2SO4.
- Cho mẫu thử nhóm (1) pư với dd BaCl2
+ Có tủa trắng: H2SO4
PT: \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
+ Không hiện tượng: HCl.
- Dán nhãn.
b, - Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa xanh: NaOH
+ Quỳ hóa đỏ: H2SO4
+ Quỳ không đổi màu: NaCl
- Dán nhãn.

hòa tan các chất vào H2O ta thu được cá dung dịch,trích mẫu thử dùng quỳ tím và dd Ba(OH)2
lấy 1 đến 2 ml các dd nhỏ vào giấy quỳ tím ta chia làm 2 nhóm:
Nhóm 1:quỳ tím từ màu tím chuyển thành màu đỏ gồm HCl và H2SO4
Nhóm 2:quỳ tím không đổi màu gồm NaCL và Na2SO4
cho nhóm 1 tác dụng với dd Ba(OH)2 nếu sau pư ở dd nào có chất rắn không tan và không bị phân hủy bởi nhiệt độ cao là BaSO4 của dd H2SO4 còn tạo dd không màu là BaCl2 của HCl
cho nhóm 2 tác dụng với dd Ba(OH)2 nếu dd nào thấy có chất rắn như khi cho nhóm 1 tác dung với Ba(OH)2 thì chất ban đầu đem pư là Na2SO4 còn không có hiện tượng gì là NaCl vì không pư với dd Ba(OH)2
-Cho quỳ tím vào 4 mẫu thử:
+Quỳ tím hóa đỏ\(\rightarrow\)HCl, H2SO4(nhóm I)
+Quỳ tím không đổi màu\(\rightarrow\)NaCl, Na2SO4(nhóm II)
-Cho dung dịch BaCl2 vào 2 mẫu nhóm I:
+Có kết tủa trắng\(\rightarrow\)H2SO4
BaCl2+H2SO4\(\rightarrow\)BaSO4\(\downarrow\)+2HCl
+Không hiện tượng\(\rightarrow\)HCl
-Cho dung dịch BaCl2 vào 2 mẫu nhóm II:
+Có kết tủa trắng\(\rightarrow\)Na2SO4
BaCl2+Na2SO4\(\rightarrow\)BaSO4\(\downarrow\)+2NaCl
+Không hiện tượng\(\rightarrow\)NaCl

PTHH:
Na2SO4 + BaCl2 ----> BaSO4\(\downarrow\) + 2NaCl
**P/s: Có thể thay BaCl2 bằng Ba(OH)2, phản ứng vẫn xảy ra tương tự.
Na2SO4 + Ba(OH)2 ---> BaSO4\(\downarrow\) + 2NaOH
Chúc em học tốt!

- Lấy mẫu thử và đánh dấu
- Cho quỳ tím vào các mẫu thử
+ Mẫu thử lam quỳ tím hóa xanh: NaOH
+ Mẫu thử làm quỳ tím hóa đỏ: H2SO4, HCl (I)
+ Mẫu thử không hiện tượng: NaCl
- Cho BaCl2 vào nhóm I
+ Mẫu thử xuất hiện kết tủa trắng: H2SO4
H2SO4 + BaCl2 \(\rightarrow\) BaSO4 + 2HCl
+ Mẫu thử không hiện tượng: HCl
H2SO4 , HCl + quỳ tím ----> đỏ
+ H2SO4 + AgNO3 ---> không có kết tủa
+ HCL + AgNO3 ----> kết tủa trắng
NaOH+ quỳ tím-----> xanh
NaCl + quỳ tím----> không có phản ứng