Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. Gọi số mol của H2, CO lần lượt là a,b.
\(\Rightarrow2a+28b=68\left(1\right)\)
\(n_{O_2\left(đktc\right)}=\dfrac{V}{22,4}=\dfrac{89,6}{22,4}=4\left(mol\right)\)
\(2H_2+O_2\rightarrow^{t^0}2H_2O\)
2 : 1 (mol)
a : \(\dfrac{a}{2}\) (mol)
\(2CO+O_2\rightarrow^{t^0}2CO_2\)
2 : 1 (mol)
b : \(\dfrac{b}{2}\) (mol)
\(\Rightarrow\dfrac{a+b}{2}=4\left(2\right)\)
-Từ (1) và (2) suy ra: \(b=2;a=6\)
\(\%m_{H_2}=\dfrac{2a}{68}.100\%=\dfrac{2.6}{68}.100\%\approx17,65\%\)
\(\%m_{CO}=\dfrac{28b}{68}.100\%=\dfrac{28.2}{68}.100\%\approx82,35\%\)
\(V_{H_2}=n.22,4=6.22,4=134,4\left(l\right)\)
\(V_{CO}=n.22,4=2.22,4=44,8\left(l\right)\)
\(\%V_{H_2}=\dfrac{134,4}{134,4+44,8}.100\%=75\%\)
\(\%V_{CO}=\dfrac{44,8}{134,4+44,8}.100\%=25\%\)

a/ \(2CO\left(0,2\right)+O_2\left(0,1\right)\rightarrow2CO_2\left(0,2\right)\)
\(2H_2\left(0,1\right)+O_2\left(0,05\right)\rightarrow2H_2O\left(0,1\right)\)
\(n_{H_2O}=\frac{1,8}{18}=0,1\)
\(n_{O_2}=\frac{3,36}{22,4}=0,15\)
Số mol O2 phản ứng ở phản ứng đầu là: \(0,15-0,05=0,1\)
\(\Rightarrow m_{CO_2}=0,2.44=8,8\)
b/ \(m_{CO}=0,2.28=5,6\)
\(m_{H_2}=0,1.2=0,2\)
c/ \(\%CO=\frac{0,2}{0,3}.100\%=66,67\%\)
\(\Rightarrow\%H_2=100\%-66,67\%=33,33\%\)

Sai đề rồi hay sao á bạn, sửa 49,6l thành 89,6l nhé!
a. PTHH: \(2H_2+O_2\rightarrow2H_2O\\ xmol:\dfrac{x}{2}mol\rightarrow xmol\)
\(2CO+O_2\rightarrow2CO_2\\ ymol:\dfrac{y}{2}mol\rightarrow ymol\)
b. Gọi x là số mol của \(H_2\) , y là số mol của \(CO\)
\(m_{hh}=m_{H_2}+m_{CO}\Leftrightarrow2x+28y=68\left(g\right)\left(1\right)\)
\(n_{O_2}=\dfrac{89,6}{22,4}=4\left(mol\right)\Leftrightarrow\dfrac{x}{2}+\dfrac{y}{2}=4\left(mol\right)\)
\(\Leftrightarrow x+y=8\left(2\right)\)
Giải (1) và (2) ta được: \(\left\{{}\begin{matrix}x=6\\y=2\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}V_{H_2}=22,4.6=134,4\left(l\right)\\V_{CO}=22,4.2=44,8\left(l\right)\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}\%V_{H_2}=\dfrac{134,4}{134,4+44,8}.100\%=75\%\\V_{CO}=25\%\end{matrix}\right.\)

Gọi: \(\left\{{}\begin{matrix}n_{CO}=x\left(mol\right)\\n_{H_2}=y\left(mol\right)\end{matrix}\right.\)
⇒ 28x + 2y = 11,8 (1)
PT: \(2CO+O_2\underrightarrow{t^o}2CO_2\)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Ta có: \(n_{O_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{CO}+\dfrac{1}{2}n_{H_2}=\dfrac{1}{2}x+\dfrac{1}{2}y\left(mol\right)\)
⇒ x + y = 0,7 (2)
Từ (1) và (2) ⇒ x = 0,4 (mol), y = 0,3 (mol)
a, \(\left\{{}\begin{matrix}\%m_{CO}=\dfrac{0,4.28}{11,8}.100\%\approx94,9\%\\\%m_{H_2}\approx5,1\%\end{matrix}\right.\)
b, Ở cùng điều kiện nhiệt độ và áp suất, % số mol cũng là % thể tích.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,4}{0,7}.100\%\approx57,14\%\\\%V_{H_2}\approx42,86\%\end{matrix}\right.\)
Bạn tham khảo nhé!
PTHH:
\(2CO+O_2\overset{t^o}{--->}2CO_2\left(1\right)\)
\(2H_2+O_2\overset{t^o}{--->}2H_2O\left(2\right)\)
Ta có: \(n_{O_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
Gọi x, y lần lượt là số mol của CO và H2
a. Theo PT(1): \(n_{O_2}=\dfrac{1}{2}.n_{CO}=\dfrac{1}{2}x\left(mol\right)\)
Theo PT(2): \(n_{O_2}=\dfrac{1}{2}.n_{H_2}=\dfrac{1}{2}y\left(mol\right)\)
\(\Rightarrow\dfrac{1}{2}x+\dfrac{1}{2}y=0,35\) (*)
Theo đề, ta có: \(28x+2y=11,8\) (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}\dfrac{1}{2}x+\dfrac{1}{2}y=0,35\\28x+2y=11,8\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,4\\y=0,3\end{matrix}\right.\)
\(\Rightarrow m_{H_2}=2.0,3=0,6\left(g\right)\)
\(\Rightarrow\%_{m_{H_2}}=\dfrac{0,6}{11,8}.100\%=5,08\%\)
\(\%_{m_{CO}}=100\%-5,08\%=94,92\%\)
b. \(\%_{V_{CO}}=\dfrac{0,4}{0,4+0,3}.100\%=57,1\%\)
\(\%_{V_{H_2}}=100\%-57,1\%=42,9\%\)

\(a)\\ 2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ 2CO + O_2 \xrightarrow{t^o} 2CO_2\)
b)
Gọi : \(n_{H_2} = a; n_{CO} = b\\ \Rightarrow 2a + 28b = 68(1)\)
Theo PTHH: \(n_{O_2} = 0,5a + 0,5b = \dfrac{89,6}{22,4} = 4(2)\)
Từ (1)(2) suy ra a = 6 ; b = 2
Vậy :
\(\%V_{H_2} = \dfrac{6}{6 + 2}.100\% = 75\%\\ \%V_{CO} = 100\% - 75\% = 25\%\)

a) 30% CO2, 10% O2, 60% N2
b) 18.03% CO2, 65,57% O2, 16.39% H2
HT
a) %VCO2= (3/3+1+6)x100= 30%
%VO2= (1/3+1+6)x100= 10%
%VN2= 100 - (30+10)= 60%
b) %mCO2= (4,4/4,4+16+4)x100= 18%
%mO2= (16/4,4+16+4)x100= 66%
%mH2= 100 - (18+66)= 16%
c)
% về thể tích cũng là % về số mol
==> %nCO2= (3/3+5+2)= 30%
%nO2= (5/3+5+2)x100= 50%
%nCO= 100-(30+50)= 20%

\(1,2H_2+O_2\underrightarrow{t}2H_2O\)
\(2Mg+O_2\underrightarrow{t}2MgO\)
\(2Cu+O_2\underrightarrow{t}2CuO\)
\(S+O_2\underrightarrow{t}SO_2\)
\(4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(C+O_2\underrightarrow{t}CO_2\)
\(4P+5O_2\underrightarrow{t}2P_2O_5\)
\(2,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(a,n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(b,n_C=0,3\left(mol\right)\Rightarrow n_{CO_2}=0,3\left(mol\right)\Rightarrow m_{CO_2}=13,2\left(g\right)\)
c, Vì\(\frac{0,3}{1}>\frac{0,2}{1}\)nên C phản ửng dư, O2 phản ứng hết, Bài toán tính theo O2
\(n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(3,PTHH:CH_4+2O_2\underrightarrow{t}CO_2+2H_2O\)
\(C_2H_2+\frac{5}{2}O_2\underrightarrow{t}2CO_2+H_2O\)
\(C_2H_6O+3O_2\underrightarrow{t}2CO_2+3H_2O\)
\(4,a,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_P=1,5\left(mol\right)\Rightarrow n_{O_2}=1,2\left(mol\right)\Rightarrow m_{O_2}=38,4\left(g\right)\)
\(b,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_C=2,5\left(mol\right)\Rightarrow n_{O_2}=2,5\left(mol\right)\Rightarrow m_{O_2}=80\left(g\right)\)
\(c,PTHH:4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(n_{Al}=2,5\left(mol\right)\Rightarrow n_{O_2}=1,875\left(mol\right)\Rightarrow m_{O_2}=60\left(g\right)\)
\(d,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(TH_1:\left(đktc\right)n_{H_2}=1,5\left(mol\right)\Rightarrow n_{O_2}=0,75\left(mol\right)\Rightarrow m_{O_2}=24\left(g\right)\)
\(TH_2:\left(đkt\right)n_{H_2}=1,4\left(mol\right)\Rightarrow n_{O_2}=0,7\left(mol\right)\Rightarrow m_{O_2}=22,4\left(g\right)\)
\(5,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=0,46875\left(mol\right)\)
\(n_{SO_2}=0,3\left(mol\right)\)
Vì\(0,46875>0,3\left(n_{O_2}>n_{SO_2}\right)\)nên S phản ứng hết, bài toán tính theo S.
\(a,\Rightarrow n_S=n_{SO_2}=0,3\left(mol\right)\Rightarrow m_S=9,6\left(g\right)\)
\(n_{O_2}\left(dư\right)=0,16875\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=5,4\left(g\right)\)
\(6,a,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_C=1,5\left(mol\right)\Rightarrow m_C=18\left(g\right)\)
\(b,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_{H_2}=0,75\left(mol\right)\Rightarrow m_{H_2}=1,5\left(g\right)\)
\(c,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_S=1,5\left(mol\right)\Rightarrow m_S=48\left(g\right)\)
\(d,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_P=1,2\left(mol\right)\Rightarrow m_P=37,2\left(g\right)\)
\(7,n_{O_2}=5\left(mol\right)\Rightarrow V_{O_2}=112\left(l\right)\left(đktc\right)\);\(V_{O_2}=120\left(l\right)\left(đkt\right)\)
\(8,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(m_C=0,96\left(kg\right)\Rightarrow n_C=0,08\left(kmol\right)=80\left(mol\right)\Rightarrow n_{O_2}=80\left(mol\right)\Rightarrow V_{O_2}=1792\left(l\right)\)
\(9,n_p=0,2\left(mol\right);n_{O_2}=0,3\left(mol\right)\)
\(PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
Vì\(\frac{0,2}{4}< \frac{0,3}{5}\)nên P hết O2 dư, bài toán tính theo P.
\(a,n_{O_2}\left(dư\right)=0,05\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=1,6\left(g\right)\)
\(b,n_{P_2O_5}=0,1\left(mol\right)\Rightarrow m_{P_2O_5}=14,2\left(g\right)\)
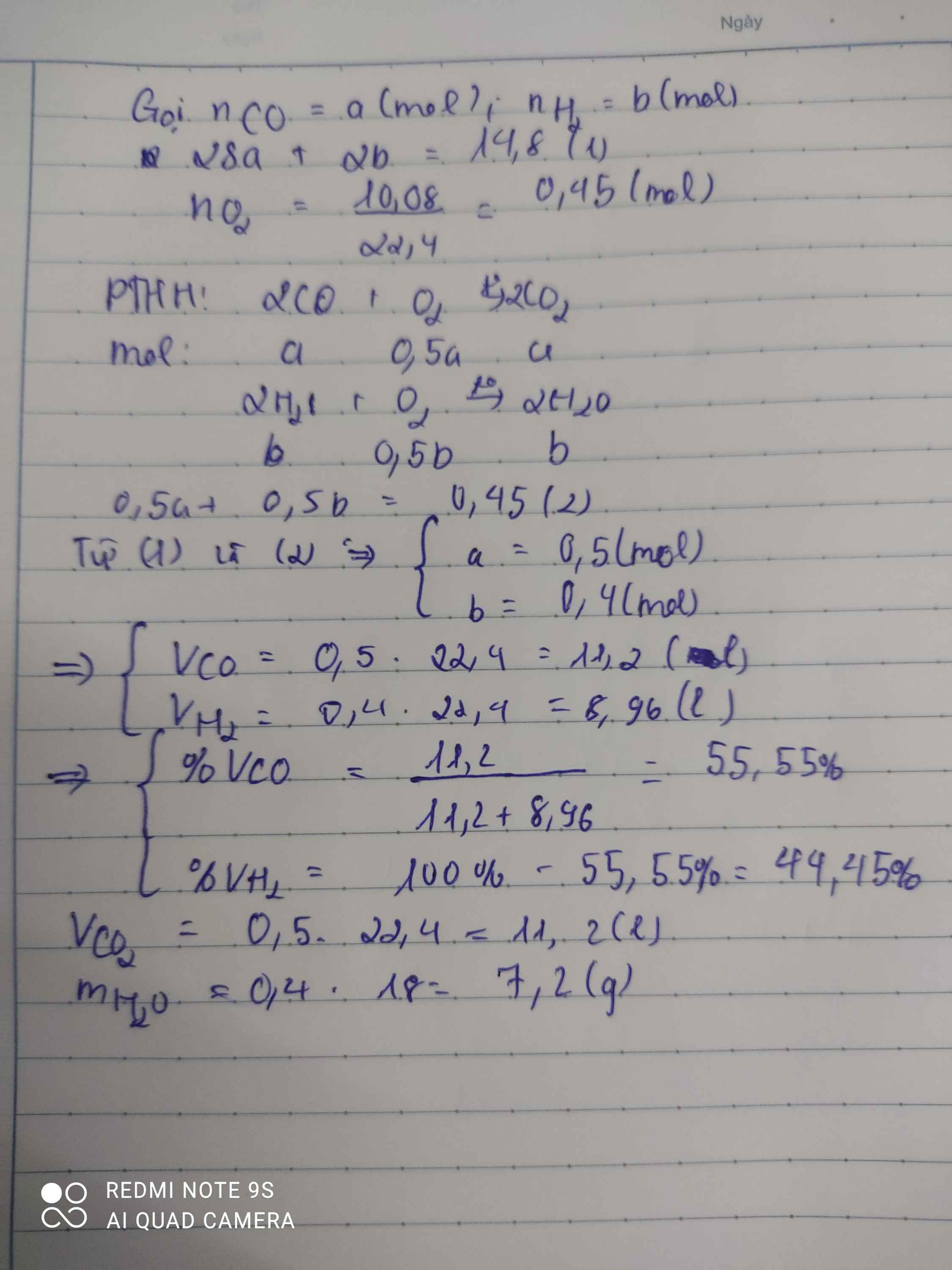
a)
Gọi số mol H2, CO là a, b (mol)
=> 2a + 28b = 68 (1)
\(n_{O_2}=\dfrac{89,6}{22,4}=4\left(mol\right)\)
PTHH: 2H2 + O2 --to--> 2H2O
a--->0,5a
2CO + O2 --to--> 2CO2
b--->0,5b
=> 0,5a + 0,5b = 4 (2)
(1)(2) => a = 6 (mol); b = 2 (mol)
\(\left\{{}\begin{matrix}\%m_{H_2}=\dfrac{6.2}{68}.100\%=17,647\%\\\%m_{CO}=\dfrac{2.28}{68}.100\%=82,353\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%V_{H_2}=\dfrac{6}{2+6}.100\%=75\%\\\%V_{CO}=\dfrac{2}{2+6}.100\%=25\%\end{matrix}\right.\)
b) Đốt cháy 2 khí trong O2 dư, dẫn sản phẩm thu được qua dd Ca(OH)2 dư:
+ Không hiện tượng: H2
2H2 + O2 --to--> 2H2O
+ Kết tủa trắng: CO
2CO + O2 --to--> 2CO2
CO2 + Ca(OH)2 --> CaCO3 + H2O