Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
Khối lượng CaO: 
Số mol CaO:
Pt:
 số mol Ca (OH)2
số mol Ca (OH)2
Vậy khối lượng Ca(OH)2tạo thành: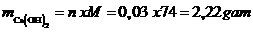
Vậy mct = 2,22 gam
 Mà
Mà 
Vậy nồng độ phần trăm Ca(OH)2: 
Câu 2:
+ Khối lượng riêng  khối lượng dd H2SO4 là
khối lượng dd H2SO4 là 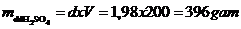
+ 
Số mol CuO: 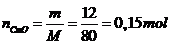
 Pt:
Pt: 

 Khối lượng
Khối lượng 
Vậy khối lượng chất tan: mct = 24 gam
Mà 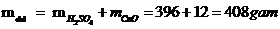
Vậy nồng độ phần trăm: 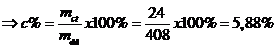

Bài 1
\(a,n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\\ CuO+2HCl\xrightarrow[]{}CuCl_2+H_2O\\ n_{CuCl_2}=n_{CuO}=0,2mol\\ m_{CuCl_2}=0,2.135=27\left(g\right)\\ b.n_{HCl}=0,2.2=0,4\left(mol\right)\\ C_{MHCl}=\dfrac{0,4}{0,5}=0,8\left(M\right)\)
Bài 5
\(a,n_{NaOH}=0,2.1=0,2\left(mol\right)\\ 2NaOH+H_2SO_4\xrightarrow[]{}Na_2SO_4+2H_2O\\ n_{H_2SO_4}=0,2:2=0,1\left(mol\right)\\ C_{MH_2SO_4}=\dfrac{0,1}{0,4}=0,25\left(M\right)\\ b,n_{Na_2SO_4}=0,2:2=0,1\left(mol\right)\\ C_{MNa_2SO_4}=\dfrac{0,1}{0,2+0,4}=\dfrac{1}{6}\left(M\right)\\ c,m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\)

Gọi nNa2CO3 = x (mol)
Na2CO3 + 2HCl \(\rightarrow\) 2NaCl + H2O + CO2
x \(\rightarrow\) 2x \(\rightarrow\) 2 x (mol)
C%(NaCl) = \(\frac{2.58,5x}{200+120}\) . 100% = 20%
=> x =0,547 (mol)
mNa2CO3 = 0,547 . 106 = 57,982 (g)
mHCl = 2 . 0,547 . 36,5 =39,931 (g)
C%(Na2CO3) =\(\frac{57,892}{200}\) . 100% = 28,946%
C%(HCl) = \(\frac{39,931}{120}\) . 100% = 33,28%

a)
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,15-->0,3----->0,15-->0,15
=> \(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
b) \(m_{FeCl_2}=0,15.127=19,05\left(g\right)\)
c) \(m_{HCl}=0,3.36,5=10,95\left(g\right)\)
=> \(C\%=\dfrac{10,95}{200}.100\%=5,475\%\)

nSO3 = \(\frac{1,2}{80}\) = 0,015 (mol)
SO3 + H2O \(\rightarrow\) H2SO4
0,015 -----------> 0,015 (mol)
a) C%(H2SO4) = \(\frac{0,015.98}{100}\) . 100% = 1,47%
b) nMgO = \(\frac{5}{40}\) = 0,125 (mol)
PT: MgO + H2SO4 \(\rightarrow\) MgSO4 + H2O
bđ 0,125 .... 0,015 (mol)
pư 0,015\(\leftarrow\) 0,015 \(\rightarrow\) 0,015 (mol)
spư 0,1125 .... 0 .............. 0,015 (mol)
Sau pư, MgO dư
mMgO = 0,1125 . 40 = 4,5 (g)
c) m dd spư = 5 + 100 - 4,5 = 100,5 (g)
C% (MgSO4)= \(\frac{0,015.120}{100,5}\) . 100% = 1,8%

a ) K2O+H2O--->2KOH
SO2+H2O--->H2SO3
N2O5+H2O-->2HNO3
b) K2O+H2SO4--->K2SO4+H2O
BaO+H2SO4-->BaSO4+H2O
Fe2O3+3H2SO4--->Al2(SO4)3+3H2O
Al2O3+6HCl--->2AlCl3+3H2O
c) SO2+2KOH-->K2SO3+H2O
Al2O3+2KOH-->2KAlO2+H2O
a) Tác dụng dduocj với nước là K2O,SO2,BaO,N2O5
K2O+H2O--->2KOH
SO2+H2O--->H2SO3
BaO+H2O--->Ba(OH)2
N2O5+H2O--->2HNO3
b) Tác dụng với H2SO4 là K20, BaO, Al2O3,Fe2O3
K2O+H2SO4--->K2SO4+H2O
BaO+H2SO4--->BaSO4+H2O
Al2O3+3H2SO4--->Al2(SO4)3+3H2O
Fe2O3+3H2SO4-->Fe2(SO4)3+3H2O
c) Tác dụng dduocj với KOH là SO2, Al2O3,
SO2+2KOH---->K2SO3+H2O
SO2+KOH-->KHSO3
Al2O3+2KOH-->2KAlO2+H2O
Bài 4 :
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(n_{Mg}=\frac{4,8}{24}=0,2\left(mol\right)\)
\(n_{H2SO4}=0,1.6=0,6\left(mol\right)\)
\(\Rightarrow\) Mg hết , H2SO4 dư
\(\Rightarrow\) Sau phản ứng trong dd gồm \(MgSO_4;H_2SO_{4_{dư}}\)
\(n_{MgSO4}=n_{Mg}=0,2\left(mol\right)\)
\(n_{H2SO4_{dư}}=0,6-0,2=0,4\left(mol\right)\)
\(CM_{MgSO4}=\frac{0,2}{0,1}=2M\)
\(CM_{H2SO4}=\frac{0,4}{0,1}=4M\)
Bài 5 :
\(FeO+2HCl\rightarrow FeCl_2+H_2O\)
\(n_{FeO}=\frac{7,2}{72}=0,1\left(mol\right)\)
\(m_{HCl}=\frac{10,95.200}{10}=21,9\left(g\right)\)
\(\Rightarrow n_{HCl}=\frac{21,9}{36,5}=0,6\left(mol\right)\)
\(\Rightarrow\) FeO hết, HCl dư
\(\Rightarrow\) Sau phản ứng trong dung dịch gồm \(FeCl_2;HCl_{dư}\)
\(C\%_{FeCl2}=\frac{0,1.127}{7,2+200}.100\%=6,1\%\)
\(C\%_{HCl}=\frac{0,4.36,4}{7,2+100}.100\%=7\%\)
Bài 5:
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
\(n_{Al}=\frac{5,4}{27}=0,2\left(mol\right)\)
\(m_{HCl}=\frac{14,6.500}{100}=73\left(g\right)\)
\(n_{HCl}=\frac{73}{36,5}=2\left(mol\right)\)
\(\Rightarrow\) Al hết, HCl dư
\(\Rightarrow\) Dung dịch sau phản ứng gồm \(HCl_{Dư};AlCl_3\)
\(C\%_{AlCl3}=\frac{0,2.133,5}{5,4+500}.100\%=5,3\%\)
\(C\%_{HCl_{Dư}}=\frac{1,4.36,5}{5,4+500}.100\%=10,11\%\)
cảm ơn bạn