Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Fe2O3+6HCl-->2FeCl3+3H2O\)
b) \(n_{Fe2O3}=\frac{48}{160}=0,3\left(mol\right)\)
\(n_{HCl}=6n_{Fe2O3}=1,8\left(mol\right)\)
\(m_{HCl}=1,8.36,5=65,7\left(g\right)\)
c) \(n_{FeCl3}=2n_{Fe2O3}=0,6\left(mol\right)\)
\(m_{FeCl3}=0,6.162,5=97,5\left(g\right)\)
a)\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
b)\(n_{Fe_2O_3}=\frac{48}{160}=0,3\left(mol\right)\)
Theo PT: \(n_{HCl}=6n_{Fe_2O_3}=1,8\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=1,8.36,5=65,7\left(g\right)\)
c) Theo PT: \(n_{FeCl_3}=2n_{Fe_2O_3}=0,6\left(mol\right)\)
\(\Rightarrow m_{FeCl_3}=0,6.162,5=97,5\left(g\right)\)

bài1
ta có dA/H2=22 →MA=22MH2=22 \(\times\) 2 =44
nA=\(\frac{5,6}{22,4}\)=0,25
\(\Rightarrow\)mA=M\(\times\)n=11 g
MA=dA/\(H_2\)×M\(H_2\)=22×(1×2)=44g/mol
nA=VA÷22,4=5,6÷22,4=0,25mol
mA=nA×MA=0,25×44=11g

Fe2O3 + 6HCl -> 2FeCl3 + 3H2O
0.3 1.8 0.6
\(nFe2O3=\dfrac{48}{160}=0.3mol\)
a.\(mFeCl3=0.6\times162.5=97.5g\)
b.\(mHCl=1.8\times36.5=65.7g\)

Bài 1: a)
nH = \(\frac{3,36}{22,4}\)= 0.15 mol
PTHH: Fe + 2HCL --> FeCl2 + H2
Pt: 1 --> 2 -------> 1 ------> 1 (mol)
PƯ: 0.15 <- 0,3 <-- 0, 15 <--- 0,15 (mol)
mHCL = n . M = 0,3 . (1 + 35,5) = 10,95 g
b) mFeCL2 = 0,15 . (56 + 2 . 35,5) = 19,05 g
mik nghĩ thế

a) %Cl = 60,68%
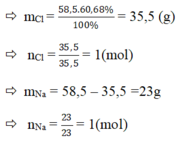
Vậy trong 1 phân tử hợp chất A có : 1 nguyên tử Na, 1 nguyên tử Cl.
⇒ CTHH của hợp chất A : NaCl
b)
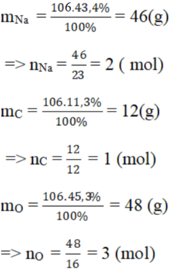
Vậy trong 1 phân tử hợp chất B có: 2 nguyên tử Na, 1 nguyên tử C, 3 nguyên tử O.
⇒ CTHH của hợp chất B : Na2CO3.

Trong 1 mol acetic acid:
\(\left\{{}\begin{matrix}m_C=60.40\%=24\left(g\right)\\m_H=60.6,67\%=4\left(g\right)\\m_O=60-24-4=32\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_C=\dfrac{24}{12}=2\left(mol\right)\\n_H=\dfrac{4}{1}=4\left(mol\right)\\n_O=\dfrac{32}{16}=2\left(mol\right)\end{matrix}\right.\)
Vậy CTHH là \(C_2H_4O_2\)

\(m_{Fe}=\%Fe.M_X=28\%.400=112\left(g\right)\\ m_S=\%S.M_X=24\%.400=96\left(g\right)\\ m_O=m_X-m_{Fe}-m_S=400-112-96=192\left(g\right)\)
\(\Rightarrow n_{Fe}=\dfrac{m}{M}=\dfrac{112}{56}=2\left(mol\right)\)
\(m_S=\dfrac{m}{M}=\dfrac{96}{32}=3\left(mol\right)\)
\(m_O=\dfrac{m}{M}=\dfrac{192}{16}=12\left(mol\right)\)
\(CTHH:Fe_2\left(SO_4\right)_3\)

a) MA = 22.2 = 44(g/mol)
b) \(m_C=\dfrac{44.27,27}{100}=12\left(g\right)=>n_C=\dfrac{12}{12}=1\left(mol\right)\)
\(m_O=44-12=32\left(g\right)=>n_C=\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH: CO2
Trong 1,5 mol khí A chứa
+ 1,5.1.6.1023 = 9.1023 nguyên tử C
+ 1,5.2.6.1023 = 18.1023 nguyên tử O
mCO2 = 1,5.44 = 66(g)
VCO2 = 1,5 . 22,4 = 33,6(l)

Bài 2
\(\%Na:\%O:\%H=57:40:3\)
\(\Rightarrow n_{Na}:n_O:n_H=\frac{57}{23}:\frac{40}{16}:\frac{3}{1}\)
\(=2,48:2,5:3\approx1:1:1\)
\(\Rightarrow CTHH:NaOH\)
Bài 3
\(Fe2O3+6HCl-->2FeCl3+3H2O\)
\(n_{FE2O3}=\frac{48}{160}=0,3\left(mol\right)\)
\(n_{FeCl3}=2n_{Fe2O3}=0,6\left(mol\right)\)
\(m_{FeCl3}=0,6.133,5=80,1\left(g\right)\)
\(n_{HCl}=6n_{Fe2O3}=1,8\left(mol\right)\)
\(m_{HCl}=1,8.36,5=65,7\left(g\right)\)