Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 14:
a) \(n_{H_2}=\dfrac{12,395}{24,79}=0,5\left(mol\right)\)
PTHH: Ca + 2H2O --> Ca(OH)2 + H2
0,5<--------------0,5<----0,5
=> mCa = 0,5.40 = 20 (g)
=> \(\left\{{}\begin{matrix}\%m_{Ca}=\dfrac{20}{34}.100\%=58,82\%\\\%m_{CaO}=100\%-58,82\%=41,18\%\end{matrix}\right.\)
b) b phải là khối lượng bazo thu được chứ nhỉ..., sao tính đc m dung dịch
\(n_{CaO}=\dfrac{34-20}{56}=0,25\left(mol\right)\)
PTHH: CaO + H2O --> Ca(OH)2
0,25---------->0,25
=> mCa(OH)2 = (0,5 + 0,25).74 = 55,5 (g)

Đặt \(n_{Fe}=x(mol);n_{Al}=y(mol)\Rightarrow 56x+27y=11(1)\)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ PTHH:Fe+H_2SO_4\to FeSO_4+H_2\\ 2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ \Rightarrow x+1,5y=0,4(2)\\ (1)(2)\Rightarrow x=0,1(mol);y=0,2(mol)\\ \Rightarrow \%_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\\ \Rightarrow \%_{Al}=100\%-50,91\%=49,09\%\)

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH:
Ca + 2H2O ---> Ca(OH)2 + H2
0,1<-------------0,1<---------0,1
=> \(\left\{{}\begin{matrix}m_{Ca}=0,1.40=4\left(g\right)\\m_{CaO}=9,6-4=5,6\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Ca}=\dfrac{4}{9,6}.100\%=41,67\%\\\%m_{CaO}=100\%-41,67\%=58,33\%\end{matrix}\right.\)
\(n_{CaO}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: CaO + H2O ---> Ca(OH)2
0,1------------------>0,1
=> \(m_{Ca\left(OH\right)_2}=\left(0,1+0,1\right).74=14,8\left(g\right)\)

Gọi \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo pt: \(\Rightarrow\left\{{}\begin{matrix}3x+y=0,2\\27x+56y=5,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{19}{470}\\y=\dfrac{37}{470}\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{\dfrac{19}{470}\cdot27}{5,5}\cdot100\%=19,84\%\)
\(\%m_{Fe}=100\%-19,84\%=80,16\%\)

a/ \(2CO\left(0,2\right)+O_2\left(0,1\right)\rightarrow2CO_2\left(0,2\right)\)
\(2H_2\left(0,1\right)+O_2\left(0,05\right)\rightarrow2H_2O\left(0,1\right)\)
\(n_{H_2O}=\frac{1,8}{18}=0,1\)
\(n_{O_2}=\frac{3,36}{22,4}=0,15\)
Số mol O2 phản ứng ở phản ứng đầu là: \(0,15-0,05=0,1\)
\(\Rightarrow m_{CO_2}=0,2.44=8,8\)
b/ \(m_{CO}=0,2.28=5,6\)
\(m_{H_2}=0,1.2=0,2\)
c/ \(\%CO=\frac{0,2}{0,3}.100\%=66,67\%\)
\(\Rightarrow\%H_2=100\%-66,67\%=33,33\%\)

a. PTHH:
\(Ca+2H_2O--->Ca\left(OH\right)_2+H_2\left(1\right)\)
\(CaO+H_2O--->Ca\left(OH\right)_2\left(2\right)\)
b. Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT(1): \(n_{Ca}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{Ca}=0,1.40=4\left(g\right)\)
\(\Rightarrow\%_{m_{Ca}}=\dfrac{4}{9,6}.100\%=41,7\%\)
\(\%_{m_{CaO}}=100\%-41,7\%=58,3\%\)
c. Ta có: \(n_{CaO}=\dfrac{9,6-4}{56}=0,1\left(mol\right)\)
Ta có: \(n_{hh}=0,1+0,1=0,2\left(mol\right)\)
Theo PT(1,2): \(n_{Ca\left(OH\right)_2}=n_{hh}=0,2\left(mol\right)\)
\(\Rightarrow m_{Ca\left(OH\right)_2}=0,2.74=14,8\left(g\right)\)

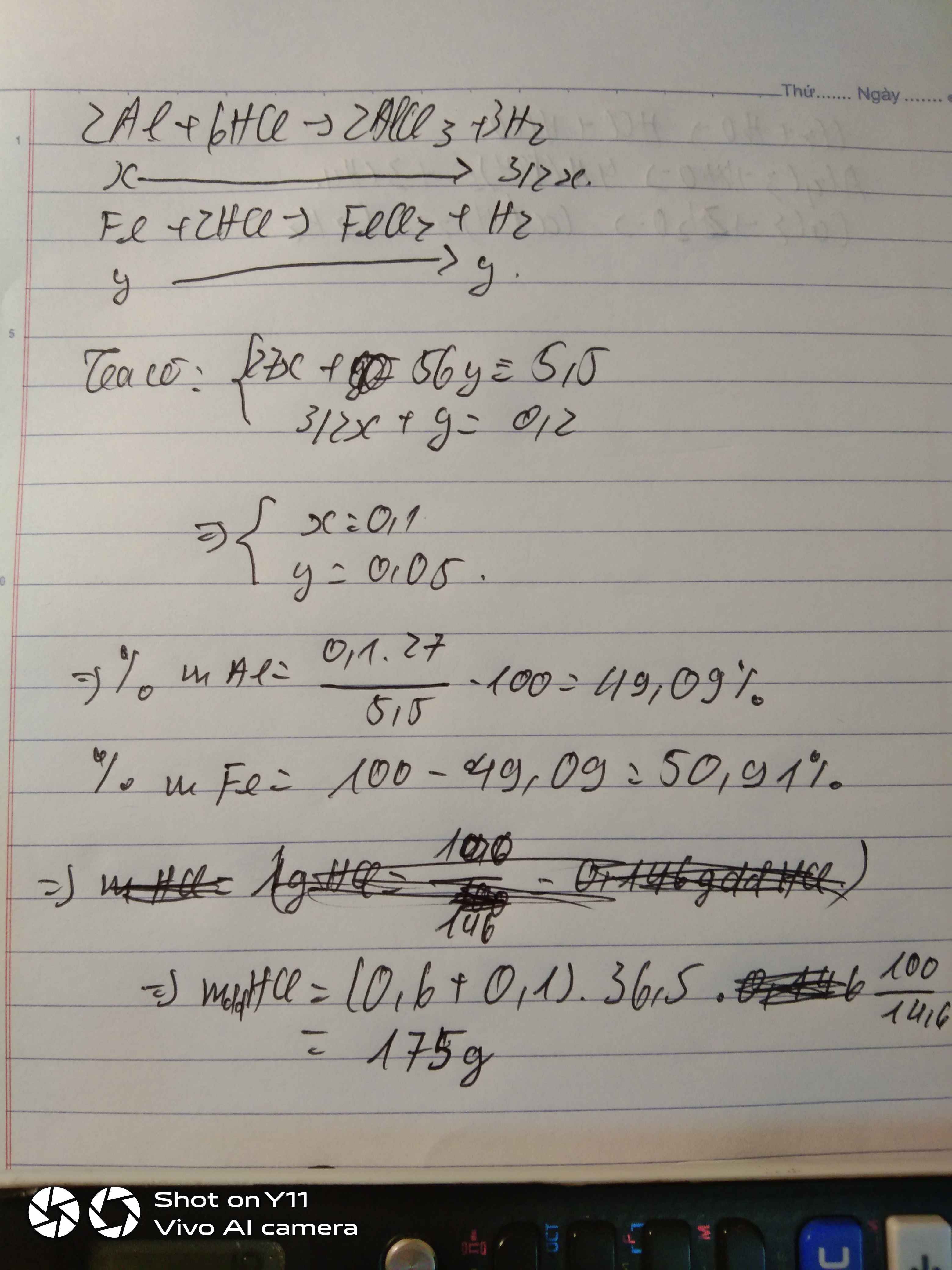


\(n_{H_2}=\dfrac{12,395}{24,79}=0,5\left(mol\right)\)
\(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\)
0,5 0,5 0,5 ( mol )
( \(CaO+H_2O\) không giải phóng \(H_2\) )
\(m_{Ca}=0,5.40=20g\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Ca}=\dfrac{20}{34}.100=58,82\%\\\%m_{CaO}=100\%-58,82\%=41,18\%\end{matrix}\right.\)
\(n_{CaO}=\dfrac{34-20}{56}=0,25\left(mol\right)\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
0,25 0,25 ( mol )
\(m_{Ca\left(OH\right)_2}=\left(0,5+0,25\right).74=55,5g\)
tk