Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a.
CO2 + Ca(OH)2 → CaCO3 + H2O
nCaCO3 = nCO2 = 0,2 => nC = 0,2
m(bình tăng) = mCO2 + mH2O
→ 44 . 0,2 + 18 . nH2O = 11,32
→ nH2O = 0,14 => nH = 0,28
Khí thoát ra là N2: nN2 = 0,02 => nN = 0,04
=> nC : nH : nN = 0,2 : 0,28 : 0,04 = 5 : 7 : 1
=> A: (C5H7N)n
Trong cafein: mN = 56 → trong nicotin mN = ½ cafein = 28 → A: có 2 nguyên tử N
Kết luận: A là C10H14N2.
b.
Tác hại của nicotin Gây xơ vữa động mạch, phì đại động mạch chủ, co thắt phế quản; gây run và đau cơ, đau khớp cũng như tăng insulin. Tác động lên đường tiêu hóa, nicotine có thể gây nôn, khô miệng, khó tiêu, tiêu chảy, ợ nóng, gây loét và ung thư. Tác động đến hệ thần kinh trung ương, nicotine có thể khiến giấc ngủ bị rối loạn, nhức đầu, chóng mặt nguy cơ hạn chế dòng máu chảy lên não, dễ bị kích thích và tăng khả năng hành động nông nổi. Nicotine làm nhịp tim có thể tăng hoặc giảm; làm tăng khả năng loạn nhịp tim; gây hẹp mạch vành, làm tăng huyết áp. Đối với người mang thai, nicotine có thể gây những tác hại như đái tháo đường type 2, béo phì, cao huyết áp, rối loạn chức năng hô hấp, khuyết tật về hành vi thần kinh và vô sinh cho đứa con trong bụng mẹ khi đã trưởng thành

Ta có: \(\left\{{}\begin{matrix}m_{H_2O}=5,4\left(g\right)\\m_{CO_2}=6,6\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\\n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_H=2n_{H_2O}=0,6\left(mol\right)\\n_C=n_{CO_2}=0,15\left(mol\right)\end{matrix}\right.\)
`=> m_C + m_H = 0,15.12 + 0,6 = 2,4 (g) = m_A`
`=> A` không chứa O
\(M_A=0,5.32=16\left(g/mol\right)\)
Ta có: \(n_C:n_H=0,15:0,6=1:4\)
`=>` CTPT của A có dạng \(\left(CH_4\right)_n\)
\(\Rightarrow n=\dfrac{16}{16}=1\)
Vậy A là CH4

a.

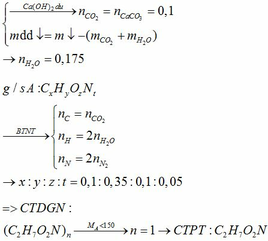
b.
Vì A pứ với NaOH nên CTCT của A là: CH3COONH4 hoặc HCOONH3CH3
Y pứ ở 15000C nên Y là: CH4
=> X: CH3COONa → A:CH3COONH4
Z: CH≡CH → T: CH3CHO
Vậy A là: CH3COONH4 (amoniaxetat)

C chứa N2, O2
Gọi \(\left\{{}\begin{matrix}n_{N_2}=x\left(mol\right)\\n_{O_2\left(dư\right)}=y\left(mol\right)\end{matrix}\right.\)
=> \(\overline{M}=\dfrac{28x+32y}{x+y}=15,2.2=30,4\left(g/mol\right)\)
=> 2,4x = 1,6y
=> 1,5x = y (1)
\(n_{H_2O}=\dfrac{9}{18}=0,5\left(mol\right)\)
Gọi số mol CO2 là z (mol)
=> \(x+y+z=\dfrac{14,56}{22,4}=0,65\left(mol\right)\) (2)
Bảo toàn C: nC(A) = z (mol)
Bảo toàn H: nH(A) = 1 (mol)
Bảo toàn N: nN(A) = 2x (mol)
\(n_{O_2\left(pư\right)}=\dfrac{13,44}{22,4}-y=0,6-y\left(mol\right)\)
Bảo toàn O: \(n_{O\left(A\right)}+2n_{O_2\left(pư\right)}=2n_{CO_2}+n_{H_2O}\)
=> \(n_{O\left(A\right)}=2y+2z-0,7\left(mol\right)\)
Do mA = 15 (g)
=> 12z + 1 + 28x + 32y + 32z - 11,2 = 15
=> 28x + 32y + 44z = 25,2 (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,15\left(mol\right)\\z=0,4\left(mol\right)\end{matrix}\right.\)
nC(A) = 0,4 (mol)
nH(A) = 1 (mol)
nO(A) = 0,4 (mol)
nN(A) = 0,2 (mol)
Xét nC(A) : nH(A) : nO(A) : nN(A) = 0,4 : 1 : 0,4 : 0,2 = 2 : 5 : 2 : 1
Mà A có 1 nguyên tử N
=> CTPT: C2H5O2N

- Sửa đề xíu 1,875 chứ không phải 1,1875
MA=1,875.32=60\(\rightarrow\)\(n_A=\dfrac{30}{60}=0,5mol\)
\(n_{CO_2}=\dfrac{22,4}{22,4}=1mol\)
\(n_{H_2O}=\dfrac{18}{18}=1mol\)
- Đặt công thức CxHyOz
CxHyOz+\(\left(x+\dfrac{y}{4}-\dfrac{z}{2}\right)\)\(\rightarrow\)xCO2+\(\dfrac{y}{2}\)H2O
x=\(\dfrac{n_{CO_2}}{n_A}=\dfrac{1}{0,5}=2\)
\(\dfrac{y}{2}=\dfrac{n_{H_2O}}{n_A}=\dfrac{1}{0,5}=2\rightarrow y=4\)
MA=12.2+4+16z=60\(\rightarrow\)16z=32\(\rightarrow\)z=2
CTPT: C2H4O2
A tác dụng NaOH nên A có thể là este hoặc axit:
Este: HCOOCH3
Axit: CH3COOH



Qui đổi ½ hh B gồm Al (x mol), Fe (y mol), O (z mol)

=> mB = 2 (mAl + mFe + mO) = 102,78g
Gọi công thức của oxit sắt là FeaOb

=> Fe2O3

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)
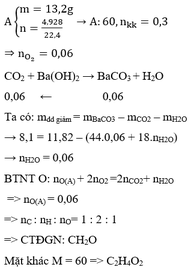
Bài 1 :
Ta có sơ đồ: \(A\underrightarrow{^{to}}B+O_2\)
\(n_{O2}=\frac{1,68}{22,4}=0,075\left(mol\right)\rightarrow m_{O2}=0,075.32=2,4\left(g\right)\)
Theo định luật bảo toàn khối lượng ta có:
mA = mB + m oxi → mB = mA - moxi
\(=15,15-2,4=12,75\left(g\right)\)
Trong B: \(m_O=12,75.37,65\%=4,8\left(g\right)\)
\(m_N=12,75.16,47\%=2,1\left(g\right)\)
\(m_K=12,75-\left(4,8+2,1\right)=5,84\left(g\right)\)
Suy ra :
\(n_O=\frac{4,8}{16}=0,3\left(mol\right)\)
\(m_N=\frac{2,1}{14}=0,15\left(mol\right)\)
\(n_K=\frac{5,85}{39}=0,15\left(mol\right)\)
Gọi CTHH của B là KxNyOz
Ta có \(x:y:z=n_K:n_N:n_O=0,15:0,15:0,3=1:1:2\)
Chọn x = 1, y = 1, z = 2 → Công thức đơn giản nhất là KNO2
Theo gt \(\rightarrow\) CTHH của B là KNO2.
Trong A: theo định luật bảo toàn nguyên tố:
\(m_O=4,8+2,4=7,2\left(g\right)\)
\(n_O=\frac{7,2}{16}=0,45\left(mol\right)\)
\(n_N=0,15\left(mol\right),n_K=0,15\left(mol\right)\)
Gọi CTHH của A là KaNbOc
Ta có\(a:b:c=0,15:0,15:0,45=1:1:3\)
Chọn a = 1, b = 1, c =3
Vậy CTHH là : \(KNO_3\)
Bài 2:
Gọi CTPT là CxHyOz
\(n_{CO2}=n_{CaCO3}=\frac{40.}{100}=0,4\left(mol\right)\)
\(m_{H2O}=26,6-0,4.44\)
\(\rightarrow n_{H2O}=0,5\)
\(n_{O2}=0,6\)
\(m_A=26,6-0,6.32=7,4\)
\(M_A=37.2=74\)
\(\rightarrow n_A=0,1\)
\(n_C=0,4\)
\(n_H=0,5.2=1\)
\(n_O=0,4.2+0,5-0,6.2\left(bt.O\right)=0,1\)
Có \(x:y:z=0,4::0,1=4:10:1\)
Vậy A là C4H10O