K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Các câu hỏi dưới đây có thể giống với câu hỏi trên

5 tháng 7 2018
Chọn đáp án A
Phản ứng: KOH + HCl → KCl + H2O
Có nKOH = 0,02 mol; nHCl = 0,01 mol
⇒ sau phản ứng thu được 200 ml dung dịch X gồm 0,01 mol KCl
và 0,01 mol KOH → dung dịch X có môi trường bazơ.
pH = 14 + log([OH−]) = 14 + log(0,01 ÷ 0,2) = 12,7 → chọn đáp án A.

3 tháng 1 2019
\(n_{NaOH}=C_M\cdot V_{NaOH}=0,2\cdot0,1=0,02\left(mol\right)\)
PTHH:\(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
Theo PTHH: \(n_{CH_3COOH}=n_{NaOH}=0,02\left(mol\right)\)
Nồng độ mol của axit axetic là:
\(C_{M_{CH_3COOH}}=\dfrac{n_{CH_3COOH}}{V_{CH_3COOH}}=\dfrac{0,02}{0,1}=0,2\left(M\right)\)
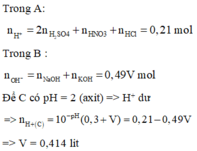

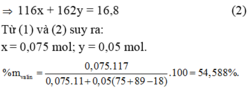
pH = 11.08
KOH + HCOOH ---> HCOOK + H2O
0,0036 0,003 mol
Theo p.ứ trên, nKOH dư = 0,0006 mol ---> pOH = -log[OH-] = -log(0,0006) = 3,22 ---> pH = 14 - pOH = 10,78.