Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Ta có: mX - mancol ban đầu = mO trong CuO phản ứng = 2,4 (g)
mancol phản ứng = nanđehit = nO trong CuO phản ứng = 2 , 4 16 = 0 , 15 ( m o l )
Lại có : nancol ban đầu > 0,15(mol) ⇒ M a n c o l < 6 , 9 0 , 15 = 46
=>ancol là CH3OH anđehit là HCHO
Vậy n A g = 4 n a n d e h i t = 0 , 6 ( m o l ) ⇒ m A g = 64 , 8 ( g )
Chú ý: Trong bài toán này ta cũng có thể nhầm lẫn nếu ngộ nhận luôn tỉ lệ tráng bạc là 1:2 . Do đó trong các bài toán về phản ứng tráng bạc của anđehit ta luôn phải xét đến trường hợp anđehit đó là HCHO.

Đáp án A
![]()
Gọi công thức chung của 2 anđehit là ![]()
Y: gồm ![]()
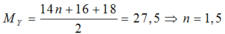
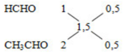
ð 2 anđehit là HCHO, CH3CHO
ð 2 ancol là CH3OH, C2H5OH
![]()

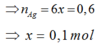
![]()

Đáp án : A
Gọi ancol là RCH2OH , ta có : RCH2OH + CuO → RCHO + H2O + Cu
Giả sử có 1 mol ancol => nRCHO = nH2O = 1
=> nY = 2 => mY = 13,75.2.2 = 55
=> mRCHO = 55 - 18 = 37
=> Andehit là HCHO và CH3CHO
Gọi nHCHO = x ; nCH3CHO = y.
Vì RCHO = 37, theo đường chéo => 7x - 7y = 0
Mặt khác : 4x + 2y = nAg = 0,6 => x = y = 0,1
Do đó, m = mCH3OH + mCH3CH2OH = 0,1.32 + 0,1.46 = 7,8

RCH2OH + CuO ![]() RCHO + Cu + H2O
RCHO + Cu + H2O
Ta có
mO trong CuO = 6,2 – 4,6 = 1,6 g
![]() nRCHO =nOtrong CuO= 1,6/16 = 0,1 mol
nRCHO =nOtrong CuO= 1,6/16 = 0,1 mol
Mặt khác, do ancol còn dư nên nancol bđ > 0,1 mol
![]()
![]()
![]() Ancol là CH3OH
Ancol là CH3OH
![]() RCHO là HCHO
RCHO là HCHO
HCHO ![]() 4Ag
4Ag
0,1 mol → 0,4 mol
![]() mAg = 108.0,4 = 43,2 g
mAg = 108.0,4 = 43,2 g
![]() Chọn C.
Chọn C.

Đáp án A
Hướng dẫn RCH2OH + O → RCHO + H2O
Bảo toàn khối lượng: mancol + mO = manđehit => nO phản ứng = (6,2 – 4,6) / 16 = 0,1 mol
=> nRCH2OH phản ứng = 0,1 mol => nRCH2OH ban đầu > 0,1 mol
=> Mancol < 4,6 / 0,1 = 46 => ancol là CH3OH => anđehit tạo ra là HCHO
nAg = 4.nHCHO = 0,4 mol => mAg = 43,2 gam

A
Sản phẩm tạo ra có phản ứng tráng bạc nên X gồm 2 ancol đơn chức.

Câu 16:
Giả sử ancol ban đầu là RCH2OH.
PT: \(RCH_2OH+CuO\underrightarrow{t^o}RCHO+Cu+H_2O\)
Có: mRCH2OH + mO (trong CuO) = mX
⇒ mO = 3,72 - 2,76 = 0,96 (g) \(\Rightarrow n_{RCH_2OH\left(pư\right)}=n_O=\dfrac{0,96}{16}=0,06\left(mol\right)\)
\(\Rightarrow n_{RCH_2OH}>0,06\left(mol\right)\)
\(\Rightarrow M_{RCH_2OH}< \dfrac{2,76}{0,06}=46\left(g/mol\right)\)
\(\Rightarrow M_R< 15\left(g/mol\right)\)
Vậy: R là H. Anđehit thu được là HCHO.
\(\Rightarrow n_{HCHO}=0,06\left(mol\right)\)
PT: \(HCHO+4AgNO_3+6NH_3+2H_2O\underrightarrow{t^o}4Ag+4NH_4NO_3+\left(NH_4\right)_2CO_3\)
Theo PT: \(n_{Ag}=4n_{HCHO}=0,24\left(mol\right)\Rightarrow m_{Ag}=0,24.108=25,92\left(g\right)\)
Đáp án: B
Câu 18:
\(m_{HCHO}=12.37,5\%=4,5\left(g\right)\Rightarrow n_{HCHO}=\dfrac{4,5}{30}=0,15\left(mol\right)\)
PT: \(HCHO+4AgNO_3+6NH_3+2H_2O\underrightarrow{t^o}4Ag+4NH_4NO_3+\left(NH_4\right)_2CO_3\)
Theo PT: \(n_{Ag}=4n_{HCHO}=0,6\left(mol\right)\Rightarrow m_{Ag}=0,6.108=64,8\left(g\right)\)
Đáp án: C

Đáp án C.
Lời giải
Hỗn hợp hơi Y gồm 2 anđehit và hơi H2O.
T a c ó n a n d e h i t = n H 2 O ⇒ M Y = M a n d e h i t + M H 2 O 2 = 13 , 75 . 2 = 27 , 5 ⇒ M a d e h i t = 37
Vì 2 ancol no, đơn chức, mạch hở, kế tiếp nhau nên 2 anđehit cũng no, đơn chức, mạch hở và kế tỉếp nhau trong dãy đồng đẳng
=> 2 anđehit là HCHO(a mol) và CH3CHO(b mol)
Ta có: M a n d e h i t = 30 a + 44 b a + b = 37 ⇒ a = b ( 1 )
Lại có n A g = 4 a + 2 b = 0 , 6 ( m o l ) ( 2 ) . Từ (1) và (2) suy ra a = b = 0,l(mol)
Vậy m = 30.0,1 + 44.0,1 = 7,4(g)
Với các bài toán cho hỗn hợp các chất và phân tử khối trung bình của chúng ta có thể dùng sơ đồ đường chéo để tính toán tỉ lệ số mol của chúng hoặc phân tử khối của chất chưa biết.

Bạn làm đc câu 3 chưa
cô giáo ơi giúp e 1 tí ạ