Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Phân tử H2 được tạo bởi 2 nguyên tử H, đều có độ âm điện là 2,2.
- Như vậy lực hút electron của 2 nguyên tử H bằng nhau. Vậy trong phân tử H2 cặp electron sẽ không bị lệch về nguyên tử nào.

- Trong phân tử NH3: độ âm điện của H và N lần lượt là 2,2 và 3,0
⟹ Nguyên tử N hút electron liên kết mạnh hơn H gấp 3,0 : 2,2 = 1,36 lần.
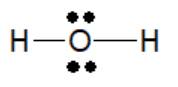
- Trong phân tử H2O: độ âm điện của H và O lần lượt là 2,2 và 3,4
⟹ Nguyên tử O hút electron liên kết mạnh hơn H gấp 3,4 : 2,2 = 1,54 lần.
Vậy cặp electron liên kết trong phân tử H2O bị lệch nhiều hơn trong phân tử H2O.

- Trong phân tử HCl, Cl có độ âm điện lớn hơn H => Cặp electron chung lệch về phía nguyên tử Cl
- Trong phân tử NH3, N có độ âm điện lớn hơn H => Cặp electron chung lệch về phía nguyên tử N
- Trong phân tử CO2, O có độ âm điện lớn hơn C => Cặp electron chung lệch về phía nguyên tử O

O3 có tính oxi hóa mạnh hơn O2 vì :
A. Số lượng nguyên tử nhiều hơn.
B. Phân tử bền vững hơn.
C. Khi phân hủy cho O nguyên tử.
D. Có liên kết cho nhận.

vì X2Y3 có 50e => 2Zx + 3Zy = 50
lại có Zx nhiều hơn Zy 5e => Zx = 13, Zy = 8
=> X:Al, Y:O
cấu hình e X: 1s22s22p63s23p1.
cấu hình e Y: 1s22s22p4

Na2O, MgO, Al2O3
SiO2, P2O5, SO3
Cl2O7
∆X
2,51 2,13 1,83
( Liên kết ion )
1,54 1,25 0,86
( Liên kết cộng hóa trị có cực)
0,28
(Liên kết cộng hóa trị không cực)
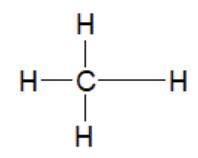
- Trong phân tử NH3: độ âm điện của H và N lần lượt là 2,2 và 3,0
⟹ Nguyên tử N hút electron liên kết mạnh hơn H gấp 3,0 : 2,2 = 1,36 lần.
- Trong phân tử H2O: độ âm điện của H và O lần lượt là 2,2 và 3,4
⟹ Nguyên tử O hút electron liên kết mạnh hơn H gấp 3,4 : 2,2 = 1,54 lần.
Vậy cặp electron liên kết trong phân tử H2O bị lệch nhiều hơn trong phân tử H2O.