Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 1: a)
nH = \(\frac{3,36}{22,4}\)= 0.15 mol
PTHH: Fe + 2HCL --> FeCl2 + H2
Pt: 1 --> 2 -------> 1 ------> 1 (mol)
PƯ: 0.15 <- 0,3 <-- 0, 15 <--- 0,15 (mol)
mHCL = n . M = 0,3 . (1 + 35,5) = 10,95 g
b) mFeCL2 = 0,15 . (56 + 2 . 35,5) = 19,05 g
mik nghĩ thế

a) PTHH: Fe + 2HCl ===> FeCl2 + H2
b) nFe = 11,2 / 56 = 0,2 (mol)
=> nH2 = nFe = 0,2 mol
=> VH2(đktc) = 0,2 x 22,4 = 4,48 lít
c) nHCl = 2.nFe = 0,4 mol
=> mHCl = 0,4 x 36,5 = 14,6 gam
d) nFeCl2 = nFe = 0,2 mol
=> mFeCl2 = 0,2 x 127 = 25,4 gam

a) Theo đề bài , ta có:
nFe= \(\frac{m_{Fe}}{M_{Fe}}=\frac{28}{56}=0,5\left(mol\right)\)
PTHH: Fe + 2HCl -> FeCl2 + H2
Theo PTHH: 1:2:1:1 (mol)
Theo đề bài: 0,5:1:0,5:0,5 (mol)
b) Theo PTHH và đề bài, ta có:
\(n_{H_2}=n_{Fe}=0,5\left(mol\right)\)
Thể tích khí H2 thu được (đktc) :
\(V_{H_2\left(đktc\right)}=n_{H_2}.22,4=0,5.22,4=11,2\left(g\right)\)
c) Theo PTHH và đề bài, ta có:
\(n_{FeCl_2}=n_{Fe}=0,5\left(mol\right)\)
Khối lượng FeCl2 thu được:
\(m_{FeCl_2}=n_{FeCl_2}.M_{FeCl_2}=0,5.127=63,5\left(g\right)\)

Bài 1.a) Số mol của Fe là:
nFe =\(\dfrac{m}{M}\) =\(\dfrac{2,8}{56}\) =0,05 (mol)
Theo phương trình hóa học Fe + HCl --->FeCl2 + H2 ta có:
nFe = nHCl =0,05 (mol)
Khối lượng của HCl là:
mHCl =n.M=0,05.36,5=1,825 (g)
b) Số mol của H2 là:
nFe = nH2 = 0,05 (mol)
Thể tích O2 thoát ra ngoài là:
VO2 = 22,4.n=22,4.0,05= 1,12 (l)

PTHH : Fe + 2HCl →FeCl2 + H2
\(n_{Fe}=\frac{m}{M}=\frac{11,2}{56}=0,2\left(mol\right)\)
\(\Rightarrow\) Từ PT \(\Rightarrow n_{Fe}=n_{H_2}=n_{FeCl_2}=0,2\left(mol\right)\)
\(n_{HCl}=n_{Fe}.2=0,2.2=0,4\left(mol\right)\)
a) \(V_{H_2}=n.22,4=0,2.22=4,48\left(l\right)\)
b) mHCl = M.n = 36,5.0,4= 14,6 (g)
c) \(m_{FeCl_2}=M.n=127.0,2=25,4\left(g\right)\)
PTHH: Fe + 2HCl ===> FeCl2 + H2
a/ nFe = 11,2 / 56 = 0,2(mol)
=> nH2 = nFe = 0,2 mol
=> VH2(đktc) = 0,2 x 22,4 = 4,48 lít
b/ nHCl = 2nFe = 0,2 x 2 = 0,4 mol
=> mHCl = 0,4 x 36,5 = 14,6 gam
c/ nFeCl2 = nFe = 0,2 mol
=> mFeCl2 = 0,2 x 25,4 gam

Khối lượng mol của khí A : dA/H2 = 17 ⇒ MA = 17.2 = 34 (g)
Khối lượng mỗi nguyên tố có trong 1 mol khí A:
 mS = 34 – 2 = 32 (g)
mS = 34 – 2 = 32 (g)
Số mol nguyên tử mỗi nguyên tố trong 1 mol khí A có:
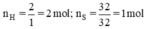
Vậy trong 1 mol phân tử chất A có : 2 nguyên tử H và 1 nguyên tử S
⇒ CTHH của khí A là H2S

Câu 1:
PTHH: Fe + 2HCl ===> FeCl2 + H2
a/ nFe = 11,2 / 56 = 0,2 mol
=> nH2 = 0,2 mol
=> VH2(đktc) = 0,2 x 22,4 = 4,48 lít
b/ => nHCl = 0,2 x 2 = 0,4 mol
=> mHCl = 0,4 x 36,5 = 14,6 gam
c/ => nFeCl2 = 0,2 mol
=> mFeCl2 = 0,2 x 127 = 25,4 gam
Câu 3/
a/ Chất tham gia: S, O2
Chất tạo thành: SO2
Đơn chất: S, O2 vì những chất này chỉ do 1 nguyên tố tạo nên
Hợp chất: SO2 vì chất này do 2 nguyên tố S và O tạo tên
b/ PTHH: S + O2 =(nhiệt)==> SO2
=> nO2 = 1,5 mol
=> VO2(đktc) = 1,5 x 22,4 = 33,6 lít
c/ Khí sunfuro nặng hơn không khí

nAl = 8,1 /27 = 0,3mol
2Al + 6HCl => 2AlCl3 + 3H2
0,3--------------->0,3------> 0,45
=> VH2 = 0,45.22,4 = 10,08 (l)
mAlCl3 = 0,3. 133,5 = 40,05 (g)

a) Có 2R+(96x3)=342
Suy ra: R=27 là nhôm(Al)
b) MB=32x0,5=16
Suy ra: MA=16x2,125=34
Ta có : HuSv
5,88%=100u/34 =>u=2
94,12%=32 x 100 x v/34 => v=1
Vậy công thức hoá học của A là: H2S
Chúc bạn học tốt!
2)M khí A= 17*2=34
cong thức tổng quát: HxSy
có:
M của H/ M khí A= % H
<=>H*x/M=5,88%
<=>1*x/34=5,88%
suy ra: x=2
=> y =1
công thức đúng là: H2S
1) Theo như SGK thì có 2,8g Fe, bạn ghi thiếu đề
a) nFe = 2,8 / 56 = 0,05 mol Phương trình hoá học: Fe + 2HCl -----> FeCl2 + H2 0, 05 mol 2.0,05 mol 0,05 mol Theo phương trình trên ta có nFe = nH = 0,05 VH2= 0,05 x 22,4 = 1,12 l. b) nHCl = 2nFe = 2 x 0,05 = 0,1 mol mHCl cần dùng: 0,1 x 36,5 = 3,65 g.