

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án B
Cho từ từ H+ vào X thì phản ứng xảy ra theo thứ tự:
H+ + CO32– → HCO3– || H+ + HCO3– → CO2 + H2O.
nCO32– = 0,1 mol; nHCO3– = 0,15 mol; nH+ = 0,2 mol.
► a = nCO2 = nH+ - nCO32– = 0,1 mol

Đặt số mol các ion trong ½ dung dịch Y là Na+: x mol; ![]()
![]()
![]()
Ø Cho từ từ 200ml dung dịch HCl 0,6M vào ½ dung dịch Y:
Số mol HCl là: ![]()
Thứ tự phản ứng: 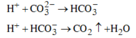
Sơ đồ phản ứng:
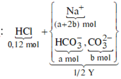
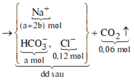
![]()
![]()
![]()
![]()
![]()
![]()
![]() => b = 0,06 mol
=> b = 0,06 mol
Ø Cho từ từ ½ dung dịch Y vào 200ml dung dịch HCl 0,6M:
Số mol HCl là: ![]()
Phương trình ion:
![]()
![]()
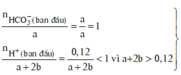


=> Tính theo H+

![]()
1/2 Y gồm ![]() Na+ : 0,16 mol
Na+ : 0,16 mol
=> Y gồm ![]() Na+ : 0,32 mol
Na+ : 0,32 mol
Ø Xét giai đoạn sục 0,32 mol CO2 vào dung dịch X:
Sơ đồ phản ứng: 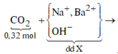
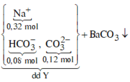
![]()
![]()
![]()
Sơ đồ phản ứng: 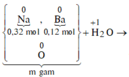
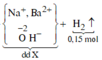
![]()
![]()
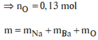
![]()
Đáp án B

Đáp án A
Hai thí nghiệm cho lượng CO2 khác nhau nên lượng H+ không dư ở cả 2 thí nghiệm.


Đáp án A
Do có khí CO2 sinh ra mà H+ hết nên Y chỉ có HCO3- và không có CO32-. (Do cho từ từ đến hết axit vào 2 muối cacbonat)
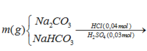
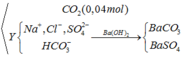
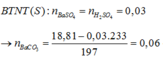
![]()
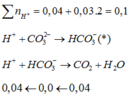
Mặt khác, n(H+) = 0,1 → n(H+) (*) = 0,06 → n(CO32-) = n(HCO3- (*)) = 0,06
→ n(Na2CO3) = 0,06 và n(NaHCO3) = 0,04 → m = 9,72