Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

H2SO4+2KOH->K2SO4+H2O
0,5-------------1
=>gồm K2SO4 và H2SO4 dư 0,05 mol
=>m K2SO4=0,5.174=87g
=>m H2SO4 dư=0,5.98=49g

\(a,4Na+O_2\underrightarrow{t^o}2Na_2O\)
\(Na_2O+H_2O\rightarrow2NaOH\)
\(b,S+O_2\underrightarrow{t^o}SO_2\)
\(SO_2+H_2O⇌H_2SO_3\)
\(c,2NaOH+H_2SO_3\rightarrow Na_2SO_3+2H_2O\)
1 1 0,5
p/u : 1 0,5 0,5
sau p/u : 0 0,5 0,5
Tên gọi Natri sunfit
Ta nhận thấy ở PT dư H2SO3 dư , nên sp tạo thành muối trung hòa ( Na2SO3)
\(m_{Na_2CO_3}=0,5.106=53\left(g\right)\)

Phương trình hóa học CaCO3 → CaO + CO2.
a) nCaO = 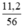 = 0,2 mol.
= 0,2 mol.
Theo PTHH thì nCaCO3 = nCaO = 0,2 (mol)
b) nCaO = 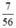 = 0,125 (mol)
= 0,125 (mol)
Theo PTHH thì nCaCO3 = nCaO = 0,125 (mol)
mCaCO3 = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO2 = nCaCO3 = 3,5 (mol)
VCO2 = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO2 = 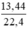 = 0,6 (mol)
= 0,6 (mol)
Theo PTHH nCaO = nCaCO3 = nCO2 = 0,6 (mol)
mCaCO3 = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)

a) \(n_{CaO}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Ta có: \(n_{CaCO_3}=n_{CaO}=0,2\left(mol\right)\)
b) \(n_{CaO}=\dfrac{7}{56}=0,125\left(mol\right)\)
Ta có : \(n_{CaCO_3}=n_{CaO}=0,125\left(mol\right)\)
=> \(m_{CaCO_3}=0,125.100=12,5\left(g\right)\)
c) \(n_{CO_2}=n_{CaCO_3}=3,5\left(mol\right)\)
=> \(V_{CO_2}=3,5.22,4=78,4\left(lít\right)\)
d) \(n_{CO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Ta có: \(n_{CO_2}=n_{CaCO_3}=n_{CaO}=0,6\left(mol\right)\)
=> \(m_{CaCO_3}=0,6.100=60\left(g\right)\)
\(m_{CaO}=0,6.56=33,6\left(g\right)\)

\(a)4K + O_2 \xrightarrow{t^o} 2K_2O\\ K_2O + H_2O \to 2KOH\\ b) 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ P_2O_5 + 3H_2O \to 2H_3PO_4\\ c) S + O_2 \xrightarrow{t^o} SO_2\\ 2SO_2 + O_2 \xrightarrow{t^o,xt} 2SO_3\\ SO_3 + H_2O \to H_2SO_4\\ Zn + H_2SO_4 \to ZnSO_4 + H_2\)

a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b, \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c, \(n_{HCl}=2n_{Mg}=0,4\left(mol\right)\Rightarrow V_{HCl}=\dfrac{0,4}{2}=0,2\left(l\right)=200\left(ml\right)\)

Ta có : \(n_{Fe2O3}=\frac{m}{M}=\frac{16}{160}=0,1\)
PTHH phản ứng : Fe2O3 + H2 -----> Fe + H2O
=> Cân bằng PTHH : Fe2O3 + 3H2 -----> 2Fe + 3H2O
Tỉ lệ hệ số chất tham 1 : 3 : 2 : 3
gia và sản phẩm 0,1 0,3 0,2 : 0,3
mol mol mol mol
=> VH2 \(=n.22,4=0,3.22,4=6,72\left(l\right)\)
=> mFe = n.M = 0,2 . 56 = 11,2 (g)
H2SO4+2KOH ->K2SO4+H2O
-> tạo ra K2SO4, KOH dư
=>m K2SO4=0,05.174=8,7g
=>m KOH dư=0,05.56=2,8g
Cho 13g kẽm vào bình chứa 500ml dd HCL tác dụng vừa đủ thu được dd A và V lít khí (đktc). tính v?