Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2Na + 2HCl => 2NaCl + H2
x/23________________x/46
2Al + 6HCl => 2AlCl3 + 3H2
x/27_________________x/18
Fe + 2HCl => FeCl2 + H2
x/56_______________x/56
x/18 > x/46 > x/56
=> Al cho nhiều H2 nhất
Gọi KL là x. (g) (x>0)
PTHH: Na + HCl -> NaCl + 1/2 H2
x/23___________________x/46(mol)
PTHH: 2 Al + 6 HCl -> 2 AlCl3 + 3 H2
x/27_______________________x/18(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
x/56_____________________x/56(mol)
Vì số mol tỉ lệ thuận thể tích : x/18 > x/46> x/56
=>Kim loại Al cho thể tích H2 lớn nhất.

Bài 1:
a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\) (2)
b, Giả sử: mZn = mAl = a (g)
\(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=\dfrac{a}{65}\left(mol\right)\\n_{Al}=\dfrac{a}{27}\left(mol\right)\end{matrix}\right.\)
Theo PT: \(\left\{{}\begin{matrix}n_{H_2\left(1\right)}=n_{Zn}=\dfrac{a}{65}\left(mol\right)\\n_{H_2\left(2\right)}=n_{Al}=\dfrac{a}{27}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{H_2\left(1\right)}< n_{H_2\left(2\right)}\)
Vậy: Al cho nhiều khí H2 hơn.
c, Giả sử: nH2 (1) = nH2 (2) = b (mol)
Theo PT: \(\left\{{}\begin{matrix}n_{Zn}=n_{H_2\left(1\right)}=b\left(mol\right)\\n_{Al}=n_{H_2\left(2\right)}=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=65b\left(g\right)\\m_{Al}=27b\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{Zn}>m_{Al}\)
Vậy: Khối lượng Al đã pư nhỏ hơn.
Bài 2:
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
a, Ta có: \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,1}{1}\), ta được Fe dư.
Theo PT: \(n_{Fe\left(pư\right)}=n_{H_2SO_4}=0,1\left(mol\right)\)
\(\Rightarrow n_{Fe\left(dư\right)}=0,1\left(mol\right)\Rightarrow m_{Fe\left(dư\right)}=0,1.56=5,6\left(g\right)\)
b, Theo PT: \(n_{H_2}=n_{H_2SO_4}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Bạn tham khảo nhé!

2) Nếu lấy cùng một khối lượng kim loại Na, Al, Fe rồi cho tác dụng lần lượt với dung dịch HCl dư thì kim loại nào cho nhiều thể tích khí H2 (đktc) nhất.
giả sử có 1 gam kim loại
2Al + 6HCl ---> 6AlCl3 + 3H2
1/27.........................................1/18
Fe + 2HCl ---> FeCl2 + H2
1/56...................................1/56
2Na + 2H2O ---> 2NaOH + H2
1/23..........................................1/46
NaOH + HCl ---> NaCl + H2O
nH2=1/18(mol) là lớn nhất
=> VH2=1/18.22,4=1,244(l)
1) Nhận biết 4 dung dịch mất nhãn đựng trong các lọ mất nhãn sau: NaOH, H2SO4, NaCl, Ba(OH)2.
trích mẫu thử
+cho quỳ tím vào các mẫu thử:
-hóa đỏ: H2SO4
-hóa xanh: NaOH và Ba(OH)2
-không đổi màu: NaCl
+cho H2SO4 vừa nhận được vào 2 chất làm quỳ tím hóa xanh:
-xuất hiện kết tủa trắng:Ba(OH)2
Ba(OH)2 + H2SO4 ---> BaSO4 + H2O
không hiện tượng: NaOH
2NaOH + H2SO4 ---> Na2SO4 + 2H2O

a) Phương trình phản ứng:
Zn + H2SO4 → ZnSO4 + H2
Fe + H2SO4loãng → FeSO4 + H2
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2
b) Giả sử cho cùng một khối lượng là a g kim loại kẽm sắt và nhôm
Zn + H2SO4 → ZnSO4 + H2 (1)
Fe + H2SO4loãng → FeSO4 + H2 (2)
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2 (3)
Ta có 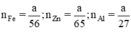
Theo pt nH2 (1) = nZn = 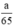 mol
mol
nH2 (2) = nFe = 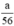 mol
mol
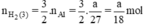
Như vậy ta nhận thấy 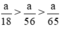 ⇒ nH2 (3) > nH2 (2) > nH2 (1)
⇒ nH2 (3) > nH2 (2) > nH2 (1)
Như vậy cho cùng một lượng kim loại tác dụng với axit H2SO4 loãng dư thì nhôm cho nhiều khí hidro hơn, sau đó đến sắt và ít nhất là kẽm
c) Nếu thu được cùng một lượng khí hidro thì khối lượng kim loại ít nhất là nhôm, sau đó đến sắt, cuối cùng là kẽm.

1)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
a. \(n_{Zn}=\frac{m}{M}=\frac{13}{65}=0,2mol\)
\(n_{HCl}=\frac{m}{M}=\frac{18,25}{36,5}=0,5mol\)
Lập tỷ lệ \(\frac{n_{Zn}}{1}\) và \(\frac{n_{HCl}}{2}\rightarrow\frac{0,1}{1}< \frac{0,5}{2}\)
Vậy sau phản ứng HCl còn dư nên tính theo số mol Zn
\(\rightarrow n_{Zn}=n_{H_2}=0,2mol\)
\(\rightarrow V_{H_2}=0,2.22,4=4,48l\)
b. Sau phản ứng thì nhúng dung dịch vào quỳ tím, làm cho quỳ tím hoá đỏ bởi còn HCl dư
c. PTHH: \(CuO+H_2\rightarrow^{t^o}Cu+H_2O\)
Trước pứ: 0,3 0,2 mol
pứ: 0,2 0,2 mol
Sau pứ: 0,1 0,2 mol
Vậy sau pứ thu được X gồm CuO dư và Cu
\(\rightarrow m_X=m_{CuO\left(dư\right)}+m_{Cu}=0,1.80+0,2.64=20,8g\)
2)
Đặt \(a\left(g\right)=m_{Na}=m_{Fe}=m_{Al}\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\left(1\right)\)
\(2Na+2HCl\rightarrow2NaCl+H_2\left(2\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\left(3\right)\)
Có \(\hept{\begin{cases}n_{Fe}=a/56mol\\n_{Al}=a/27mol\\n_{Na}=a/23mol\end{cases}}\)
Theo phương trình \(n_{H_2}\left(1\right)=\frac{3}{2}n_{Al}=\frac{a}{18}mol\)
\(n_{H_2}\left(2\right)=\frac{1}{2}n_{Na}=\frac{a}{46}mol\)
\(n_{H_2}\left(3\right)=n_{Fe}=\frac{a}{56}mol\)
\(\frac{a}{18}\approx0,056a\left(mol\right)\)
\(\frac{a}{46}\approx0,22a\left(mol\right)\)
\(\frac{a}{56}\approx0,018a\left(mol\right)\)
Xét \(0,018a< 0,22a< 0,056a\)
Vậy Al cho thể tích \(H_2\) là nhiều nhất.
sao ngọc nam chưa nổi 1000 điểm mà được làm cộng tác viên rồi

a)
\(Zn+H2SO4\rightarrow ZnSO4+H2\)
\(2Al+3H2SO4\rightarrow Al2\left(SO4\right)3+3H2\)
\(Fe+H2SO4\rightarrow FeSO4+H2\)
b) giải sử khối KL cùng là \(m\left(g\right)\)
\(\Rightarrow n_{Zn}=\frac{m}{65}\Rightarrow n_{H_2}=\frac{m}{65}\)
\(\Rightarrow n_{Al}=\frac{m}{27}\Rightarrow n_{H_2}=1,5.\frac{m}{27}\)
\(\Rightarrow n_{Fe}=\frac{m}{56}\Rightarrow n_{H_2}=\frac{m}{56}\)
\(\Rightarrow Al\)
c) Giả sử : \(n_{H_2}=0,15mol\)
\(\Rightarrow n_{Zn}=0,15mol\Rightarrow m=9,75g\)
\(\Rightarrow n_{Al}=0,1mol\Rightarrow m=2,7g\)
\(\Rightarrow n_{Fe}=0,15mol\Rightarrow m=8,4g\)
\(\Rightarrow Al\)

a)
$Zn + H_2SO_4 \to ZnSO_4 + H_2(1)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2(2)$
$Fe + H_2SO_4 \to FeSO_4 + H_2(3)$
b)
Coi m Zn = m Al = m Fe = 100(gam)
\(n_{H_2(1)} = n_{Zn} = \dfrac{100}{65}(mol)\\ n_{H_2(2)} = \dfrac{3}{2}n_{Al} = \dfrac{3}{2}.\dfrac{100}{27} = \dfrac{100}{18}(mol)\\ n_{H_2(3)} = n_{Fe} = \dfrac{100}{56}(mol)\\\)
Ta thấy :
\(n_{H_2(1)} < n_{H_2(3)} < n_{H_2(2)}\) nên dùng kim loại Al cho được nhiều khí hidro nhất.
c) Coi $n_{H_2} = 1(mol)$
n Zn = n H2 = 1(mol) => m Zn = 1.65 = 65(gam)
n Al = 3/2 n H2 = 1,5(mol) => m Al = 1,5.27 = 40,5(gam)
n Fe = n H2 = 1(mol) => m Fe = 1.56 = 56(gam)
Vậy cùng một thể tích hidro thì Al có khối lượng nhỏ nhất
a, PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\) (1)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\) (2)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\) (3)
b, Giả sử: mZn = mAl = mFe = a (g)
\(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=\dfrac{a}{65}\left(mol\right)\\n_{Al}=\dfrac{a}{27}\left(mol\right)\\n_{Fe}=\dfrac{a}{56}\left(mol\right)\end{matrix}\right.\)
Theo PT: \(\left\{{}\begin{matrix}n_{H_2\left(1\right)}=n_{Zn}=\dfrac{a}{65}\left(mol\right)\\n_{H_2\left(2\right)}=\dfrac{3}{2}n_{Al}=\dfrac{a}{18}\left(mol\right)\\n_{H_2\left(3\right)}=n_{Fe}=\dfrac{a}{56}\left(mol\right)\end{matrix}\right.\)
⇒ Al cho nhiều khí H2 nhất.
c, Giả sử: nH2 (1) = nH2 (2) = nH2 (3) = b (mol)
Theo PT: \(\left\{{}\begin{matrix}n_{Zn}=n_{H_2\left(1\right)}=b\left(mol\right)\\n_{Al}=\dfrac{2}{3}n_{H_2\left(2\right)}=\dfrac{2}{3}b\left(mol\right)\\n_{Fe}=n_{H_2\left(3\right)}=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=65b\left(g\right)\\m_{Al}=\dfrac{2}{3}b.27=18b\left(g\right)\\m_{Fe}=56b\left(g\right)\end{matrix}\right.\)
⇒ Khối lượng Al pư là nhỏ nhất.

gọi số mol của 3 chất = nhau là a (mol) (a>0)
\(pthh:Fe+2HCl\rightarrow FeCl_2+H_2\) (1)
a a
\(pthh:2Al+6HCl\rightarrow2AlCl_3+3H_2\) (2)
a \(\dfrac{3}{2}a\)
\(pthh:Na+HCl\rightarrow NaCl+\dfrac{1}{2}H_2\) (3)
a \(\dfrac{1}{2}a\)
nhận xét : phản ứng (2) cho nhiều VH2 nhiều nhất
\(n_{Al}=\dfrac{a}{27}\left(mol\right)\\ n_{Fe}=\dfrac{a}{56}\left(mol\right)\\ n_{Na}=\dfrac{a}{23}\left(mol\right)\\ pthh:Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(\dfrac{a}{56}\) \(\dfrac{a}{56}\)
\(pthh:2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\) (2)
\(\dfrac{a}{27}\) \(\dfrac{a}{18}\)
\(pthh:Na+HCl\rightarrow NaCl+\dfrac{1}{2}H_2\uparrow\) (3)
\(\dfrac{a}{23}\) \(\dfrac{a}{46}\)
nhận xét : pt (2) cho nhiều H2 nhất