Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Hỗn hơp X gồm: \(\left\{{}\begin{matrix}C_nH_{2n+2}:a\left(mol\right)\\C_mH_{2m-2}:b\left(mol\right)\end{matrix}\right.\)
Ta có: \(\dfrac{14n+2}{14m-2}=\dfrac{22}{13}\)
\(\Leftrightarrow182n+26=308m-44\)
\(\Leftrightarrow182n-308m=-70\)\(\left(I\right)\)
Khi đốt cháy hoàn toàn 0,2 mol hỗn hợp X thì:
Ta có: \(a+b=0,2\) \((II)\)
\(C_nH_{2n+2}\left(a\right)+\left(\dfrac{3n+1}{2}\right)O_2-t^o->nCO_2\left(an\right)+\left(n+1\right)H_2O\left(an+a\right)\)
\(C_mH_{2m-2}\left(b\right)+\left(\dfrac{3m-1}{2}\right)O_3-t^o->mCO_3\left(bm\right)+\left(m-1\right)H_2O\left(bm-b\right)\)
\(n_{CO_2}=0,5\left(mol\right)\)
\(\Rightarrow an+bm=0,5\)\((III)\)
\(n_{H_2O}=0,5\left(mol\right)\)
\(\Rightarrow an+bm+a-b=0,5\)\((IV)\)
Thay (III) vào (IV), ta được: \(a-b=0\) \((V)\)
Từ (II) và (V) => \(\left\{{}\begin{matrix}a+b=0,2\\a-b=0\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
Thay vào (III), ta được: \(0,1n+0,1m=0,5\)\(\left(VI\right)\)
Từ (I) và (VI) => \(\left\{{}\begin{matrix}182n-308m=-70\\0,1n+0,1m=0,5\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}n=3\\m=2\end{matrix}\right.\)
\(\Rightarrow A\left\{{}\begin{matrix}C_3H_8\\C_2H_2\end{matrix}\right.\)

B
Có mH = mT → 0,2. MH = nT. MT → nT = 0,2. 3/4= 0,15 mol
Có nH2 pư = nH - nT = 0,2 - 0,15 = 0,05 mol
Có nX + 2nY = 0,05 → nX + nY < 0,05 → 0,2 > nH2 ban đầu > 0,2 - 0,05 = 0,15 mol
0,2 - 0,05> nH2 dư > 0,15- 0,05 → 0,15> nH2 dư > 0,1
Vậy chỉ có B thỏa mãn. Đáp án B

Câu 4:
\(\overline{M_O}=6,2.2=12,4\)
Gọi a, b là mol mỗi khí ban đầu
\(\Rightarrow\frac{28a+2b}{a+b}=12,4\Leftrightarrow15,6a=10,4b\)
\(\Rightarrow\frac{a}{b}=\frac{2}{3}\)
Giả sử a=2; b=3
\(C_2H_4+H_2\underrightarrow{^{to}}C_2H_6\)
Theo lí thuyết có 2 mol H2 phản ứng
\(m_{hh}=2.28+3.2=62\left(g\right)\)
Sau phản ứng:
\(\overline{M}=8,86.2=17,72\left(g\right)\)
\(n=\frac{62}{17,72}=3,5\left(mol\right)\)
Trước phản ứng: n0 = 5mol
\(\Rightarrow n_{giam}=1,5\left(mol\right)=n_{H2\left(pư\right)}\)
\(\Rightarrow H=\frac{1,5.100}{2}=75\%\)

Gọi số mol N2 và H2 là a, b (mol)
Ta có: \(\frac{28a+2b}{a+b}=7,2=>4a=b\)
=> \(\left\{{}\begin{matrix}n_{N_2}=a\left(mol\right)\\n_{H_2}=4a\left(mol\right)\end{matrix}\right.\)
Gọi k là hiệu suất => \(n_{N_2\left(pư\right)}=ak\left(mol\right)\)
PTHH: \(N_2+3H_2\rightarrow2NH_3\)
Trc pư:_a____4a_______0_____(mol)
Pư _ak--->3ak------>2ak____(mol)
Sau pư:(a-ak)_(4a-3ak)__2ak___(mol)
= >\(\frac{28\left(a-ak\right)+2\left(4a-3ak\right)+17.2ak}{\left(a-ak\right)+\left(4a-3ak\right)+2ak}=8\)
=> k = 0,25 = 25%

ta có :2NaNO3=> 2NaNO2+O2
x------------------------->0,5x
2Zn(NO3)2=>2ZnO+4NO2+O2
y----------------------->2y----->0,5y
ta có hệ : \(\begin{cases}85x+189y=31,65\\16x+108y=40,6154\end{cases}\)
giải hệ ra đc x và y
và y là số mol của Zn(NO3)2
=> khối lượng

a.
Quy về chất đầu dãy đồng đẳng, quy đổi hỗn hợp M thành: \(\left\{{}\begin{matrix}C_2H_2\\OHC-CHO\\CH_2\end{matrix}\right.\)
Đặt số mol mỗi chất lần lượt là x, y, z (mol)
Theo đề ra ta có hệ phương trình:
26x + 58y + 14z = 18,4 (bảo toàn khối lượng)
2x + 2y + z = 0,8 (bảo toàn C)
10x + 6y + 6y = 0,75.4 (bảo toàn electron)
Suy ra \(\left\{{}\begin{matrix}x=0,15\\y=0,25\\z=0\end{matrix}\right.\) vậy nên ankin là C2H2 còn anđehit là OHC-CHO
b. 36,8 = 2.18,4 nên số mol anđehit là 0,25.2 = 0,5 (mol)
Vì có hai nhóm -CHO nên nAg =4nandehit = 0,5.4 = 2 (mol) \(\rightarrow\) 216 (g) Ag

1)Hỗn hợp khí A : CnH2n (b mol ) và H2 ( a mol )
d A/H2 = 9,1 => MA/MH2 = 9,1 (1)
Không làm mất màu Brom đó là Ankan
CnH2n + H2 -(Ni , t°)-> CnH2n+2
b ---------> b ----------> b (mol)
Hỗn hợp khí B là : CnH2n+2 ( b mol ) và H2 dư ( a - b ) (mol)
d B/H2 = 13 => MB/MH2 = 13 (2)
Từ (1) , (2) => MA / 9,1 = MB / 13
<=> mA / nA.9,1 = mB / nA.13
Mà định luật bảo toàn khối lượng : mA = mB
<=> nA.9,1 = nB.13
<=> (a + b).9,1 = (a - b + b ).13
<=> 9,1a + 9,1b = 13a
<=> 9,1b = 3,9a
<=> a = 7/3b
Mà MA = (14n.b + 2a) / a + b = 9,1 x 2 = 18,2
<=> 14nb + 14/3b / 7/3b + b = 18,2
<=> 14b(n + 1/3) / 10/3b = 18,2
<=> 21/5(n + 1/3) = 18,2
<=> n + 1/3 = 13/3
<=> n = 4
=> Đó là C4H8
Mà khả năng cộng với HBr ra 1 sản phẩm duy nhất.
CH3 - CH = CH - CH3
3 sd PP đường chéo => n H2 : n C2H4 = 1:1,
coi n H2 = n C2H4 = 1 mol
g/s sau P.ư tọa ra a mol C2H6
=> n H2 = n C2H2 = 1-a
khối lượng TB M=m/n=20 giải ra => a=0,5
=> H=50%

Đáp án B
hhM gồm CnH2n - 2 và H2 có dM/CH4 = 0,6.
Nung M với Ni → hhN có N/CH4 = 1.
• Ta có hhN có M = 16 → H2 dư.
Đặt nCnH2n - 2 x mol và H2 y mol.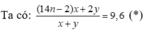
Vì phản ứng xảy ra hoàn toàn → hhN gồm CnH2n + 2 x mol và H2 dư (y - 2x) mol.![]()
Từ (*), (**) → y = 4x → n = 3 → CH≡C-CH3 → metylaxetilen

