Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tính toán theo PTHH :
Mg + CuSO4 → Cu + MgSO4
Mg + FeSO4 → Fe + MgSO4
Ba(OH)2 + MgSO4 → BaSO4 + Mg(OH)2
Ba(OH)2 + FeSO4 → BaSO4 + Fe(OH)2
Mg(OH)2 → MgO + H2O
2 Fe(OH)2 + ½ O2 → Fe2O3 + 2 H2O
Giả sư dung dịch muối phản ứng hết
=> n Fe = n FeSO4 = 0,2 . 1= 0,2 mol => m Fe = 0,2 . 56 = 11,2 g
=> n Cu =n CuSO4 = 0,2 . 0,5 = 0,1 mol => m Cu = 0,1 . 64 = 6,4 g
=> m chất rắn = 11,2 + 6,4 = 17,6 g > 12 g > 6,4
=> kim loại Fe dư sau phản ứng Vì CuSO4 phản ứng trước sau đó mới đến FeSO4 phản ứng
CuSO4 đã hết và phản ứng với 1 phần FeSO4
12 g = m Cu + m Fe phản ứng = 6,4 g + m Fe phản ứng
=> m Fe = 5,6 g => n Fe = 0,1 mol => n FeSO4 dư = 0,2 – 0,1 = 0,1 mol
Theo PTHH : n Mg = 0,1 + 0,1 = 0,2 mol ( bắng số mol CuSO4 và FeSO4 phản ứng )
Theo PTHH : n Mg = n MgSO4 = n Mg(OH)2 = n MgO = 0,2 mol
n FeSO4 dư = n Fe(OH)2 = n Fe2O3 . 2 = 0,1 mol
=> n Fe2O3 = 0,1 mol
=> m chất rắn = m Fe2O3 + m MgO = 0,1 . 160 + 0,2 . 40 = 24 g
$n_{CuSO_4} = 0{,}2 \times 0{,}5 = 0{,}1 \text{ mol}$ $n_{FeSO_4} = 0{,}2 \times 1 = 0{,}2 \text{ mol}$ Phản ứng với Mg: $Mg + CuSO_4 \rightarrow MgSO_4 + Cu \downarrow$ $Mg + FeSO_4 \rightarrow MgSO_4 + Fe \downarrow$ Khối lượng chất rắn $X$: $m_{Cu} = 0{,}1 \times 63{,}5 = 6{,}35 \text{ g}$ $6{,}35 + 56x = 12 \Rightarrow x = 0{,}101 \text{ mol}$ (số mol Fe tạo ra) Số mol Fe còn lại trong dung dịch: $n_{Fe^{2+}} = 0{,}2 - 0{,}101 = 0{,}099 \text{ mol}$ Kết tủa $E$ tạo thành khi cho dung dịch Y tác dụng với Ba(OH)$2$: $n{Fe(OH)2} = 0{,}099 \text{ mol}$ $m{Fe(OH)_2} = 0{,}099 \times 90 = 8{,}91 \text{ g}$ Nung $E$ tạo Fe$2$O$3$: $n{Fe_2O_3} = \dfrac{0{,}099}{2} = 0{,}0495 \text{ mol}$ $m{Fe_2O_3} = 0{,}0495 \times 160 = 7{,}92 \text{ g}$

Phương trình:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
FeSO4 + 2NaOH → Na2SO4 + Fe(OH)2↓
Fe2(SO4)3 + 6NaOH → 3Na2SO4 + 2Fe(OH)3↓
2Fe(OH)2 + ½ O2 → Fe2O3 + 2H2O
2Fe(OH)3 → Fe2O3 + 3H2O
Fe2O3 + 3CO → 2Fe + 3CO2↑
CO2 + Ca(OH)2 → CaCO3↓ + H2O
3CO2 + Ca(OH)2 → Ca(HCO3)2
Ca(HCO3)2 → CaCO3 + CO2↑ + H2O

nHCl = 0,4.0,5 = 0,2 mol; nH2SO4 = 0,08.0,5 = 0,04 mol
nH+ = nHCl + 2nH2SO4 = 0,28 mol
Đặt số mol của Zn và Mg trong hỗn hợp ban đầu là x và y (mol)
Ta có: 65x + 24y = 5,34 (1)
Zn + 2H+ → Zn2+ + H2
x → 2x → x (mol)
Mg + 2H+ → Mg2+ + H2
y → 2y → y (mol)
Dung dịch Y gồm có:
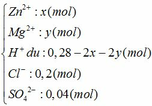
Ta thấy: nH+ + 2nZn2+ + 2nMg2+ (= 0,28 mol) < nNaOH (= 0,3 mol)
=> NaOH dư, Zn(OH)2 bị tan một phần
=> nNaOH hòa tan kết tủa = 0,3 – 0,28 = 0,02 mol
H+ + OH- → H2O
0,28-2x-2y → 0,28-2x-2y (mol)
Zn2+ + 2OH- → Zn(OH)2
x → 2x → x (mol)
Mg2+ + 2OH- → Mg(OH)2
y → 2y → y (mol)
Zn(OH)2 + 2OH- → ZnO22- + H2O
0,01 ← 0,02 (mol)
Khối lượng kết tủa thu được sau phản ứng: m kết tủa = mMg(OH)2 + mZn(OH)2
=> 99(x-0,01) + 58y = 8,43 <=> 99x + 58y = 9,42 (2)
Từ (1) và (2) ta có:

Ta có: nKOH : nBa(OH)2 = 0,4:0,05 = 8
Giả sử số mol của KOH và Ba(OH)2 lần lượt là 8a và a (mol)
=> nBa2+ = a (mol); nOH- = nKOH + 2nBa(OH)2 = 10a (mol)
- Khi kết tủa Mg(OH)2 và Zn(OH)2 đạt giá trị lớn nhất: nOH- = nH+ dư + 2nZn2+ + 2nMg2+
=> 10a = 0,04 + 2.0,06 + 2.0,06 => a = 0,028 mol
Ta thấy a < nSO42- => BaSO4 chưa đạt cực đại
- Giả sử sau khi Mg(OH)2 và Zn(OH)2 đạt cực đại ta thêm 8b mol KOH và b mol Ba(OH)2:
+ Lượng kết tủa sinh thêm là lượng BaSO4: nBaSO4 = nBa(OH)2 = b mol
=> mBaSO4 = 233b (gam)
+ Lượng kết tủa bị tan ra: nZn(OH)2 = nOH-: 2 = 10b : 2 = 5b (mol)
=> mZn(OH)2 = 99.5b = 495b (gam)
Ta thấy khối lượng kết tủa sinh ra nhỏ hơn khối lượng kết tủa bị tan nên khối lượng kết tủa lớn nhất là thời điểm Mg(OH)2 và Zn(OH)2 đạt cực đại. Khi đó: nBa(OH)2 = a = 0,028 mol
=> V = 0,028 : 0,05 = 0,56 (lít)
Kết tủa sau phản ứng gồm có:
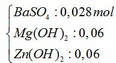
Mg(OH)2 → t ∘ MgO + H2O
0,06 mol → 0,06 mol
Zn(OH)2 → t ∘ ZnO + H2O
0,06 mol → 0,06 mol
=> m = mBaSO4 + mMgO + mZnO = 0,028.233 + 0,06.40 + 0,06.81 = 13,784 gam

- Phần 1 tác dụng với Br2: nBr2 = 16:160 = 0,1 mol
C2H2 + 2Br2 → C2H2Br4
0,05 ← 0,1 (mol)
- Đặt số mol khí mỗi phần như sau:
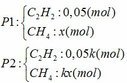
+ Số mol hỗn hợp khí X là: nX = 11,2:22,4 = 0,5 mol
Ta có: n khí P1 + n khí P2 = nX => 0,05 + x + 0,05k + kx = 0,5 <=> (x + 0,05)k = 0,45 - x
=> 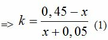
+ Đốt cháy phần 2:
C2H2 + 2,5O2 → t ∘ 2CO2 + H2O
0,05k → 0,1k→ 0,05k (mol)
CH4 + 2O2 → t ∘ CO2 + 2H2O
kx → kx → 2kx (mol)
Sản phẩm cháy gồm
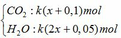
dẫn qua dung dịch Ba(OH)2 dư:
CO2 + Ba(OH)2 → BaCO3↓ + H2O
k(x+0,1) → k(x+0,1) (mol)
Khối lượng dung dịch giảm: m dd giảm = mBaCO3 – mCO2 – mH2O
=> 197k(x+0,1) – 44k(x+0,1) – 18k(2x+0,05) = 69,525
=> 153k(x+0,1) – 18k(2x+0,05) = 69,525
=> k(117x+14,4) = 69,525
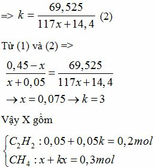
CaC2 + 2H2O → Ca(OH)2 + C2H2
0,2 ← 0,2 (mol)
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
0,1 ← 0,1 (mol)
Giá trị của m là: m = mCaC2 + mAl4C3 = 0,2.64 + 0,1.144 = 27,2 gam
Phần trăm thể tích các khí trong X là:

tác dụng với AgNO3 trong NH3 dư:
C2H2 + 2AgNO3 + 2NH3 → Ag2C2↓ + 2NH4NO3
0,15 → 0,15 (mol)
Khối lượng kết tủa thu được là: mAg2C2 = 0,15.240 = 36 gam

Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
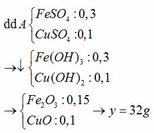






Bài 1:
1.
\(BaCl_2+2AgNO_3\rightarrow Ba\left(NO_3\right)_2+2AgCl\)
\(KCl+AgNO_3\rightarrow KNO_3+AgCl\)
\(MgCl_2+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2AgCl\)
\(Fe+2AgNO_3\rightarrow Fe\left(NO_3\right)_2+2Ag\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Mg\left(NO_3\right)_2+2NaOH\rightarrow Mg\left(OH\right)_2+2NaNO_3\)
\(Fe\left(NO_3\right)_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaNO_3\)
\(Mg\left(OH\right)_2\underrightarrow{^{to}}MgO+H_2O\)
\(2Fe\left(OH\right)_2+\frac{1}{2}O_2\rightarrow Fe_2O_3+2H_2O\)
Ta có :
\(n_{Fe}=\frac{22,4}{56}=0,4\left(mol\right)\)
\(n_{H2}=0,2\left(mol\right)\rightarrow n_{Fe_{du}}=0,2\left(mol\right)\rightarrow n_{Fe_{pu}}=0,2\left(mol\right)\)
\(\rightarrow n_{AgNO_3}=0,4\left(mol\right)\)
\(\Sigma n_{AgNO3}=1,2\left(mol\right)\rightarrow n_{AgNO3_{pu}}=0,8\left(mol\right)=n_{AgCl}\)
\(\rightarrow m_Y==m_{AgCl}=114,8\left(g\right)\)
E gồm 0,2 (mol) Fe dư , 0,4 (mol) Ag \(\rightarrow m_E=54,4\left(g\right)\)
2. Gọi a ,b ,c là số mol của BaCl2 ; KCl ; MgCl2
\(\rightarrow208a+74,5b+95c=54,7\left(1\right)\)
\(2a+b+2c=0,8\left(2\right)\)
\(Mg\left(NO_3\right)_2\rightarrow Mg\left(OH\right)_2\rightarrow MgO\)
b________________________b
\(Fe\left(NO_3\right)_2\rightarrow Fe\left(OH\right)_2\rightarrow Fe_2O_3\)
0,2_______________________0,1
\(\rightarrow40b+160.0,1=24\left(3\right)\)
Từ ( 1 ) , ( 2 ) , ( 3 ) \(\rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\\c=0,2\end{matrix}\right.\)
\(\rightarrow\%_{BaCl2}=\frac{0,1.108.100}{54,7}=38\%\)
\(\%_{KCl}=\frac{0,2.74,5.100}{54,7}=27,24\%\)
\(\%_{MgCl2}=100\%-\left(38\%+27,24\%\right)=34,76\%\)